
| A. | 钢制品应接电源的正极 | |
| B. | 电镀时铝作阳极,阳极反应式为Al-3e-+7AlCl4-=4Al2Cl7- | |
| C. | 电解液中H+移向阴极,OH-移向阳极 | |
| D. | 每生成1mol铝,电解液中转移3mol电子 |
分析 A、在钢制品上电镀铝,应让铝做阳极;
B、电解时铝做阳极,铝本身失电子放电;
C、电解液为非水体系,是由有机阳离子、Al2Cl7-和AlCl4-组成的离子液体;
D、根据阴极反应为:4Al2Cl7-+3e-=Al+7AlCl4-来分析.
解答 解:A、在钢制品上电镀铝,应让铝做阳极,即铝连电源的正极,故A错误;
B、电解时铝做阳极,铝本身失电子放电,在有机阳离子、Al2Cl7-和AlCl4-组成的离子液体中,电极反应式为:Al-3e-+7AlCl4-=4Al2Cl7-,故B正确;
C、电解液为非水体系,是由有机阳离子、Al2Cl7-和AlCl4-组成的离子液体,无H+和OH-,故C错误;
D、在阴极上,Al2Cl7-放电得金属铝,阴极反应为:4Al2Cl7-+3e-=Al+7AlCl4-,故生成1mol铝时转移3mol电子,故D正确.
故选BD.
点评 本题考查了电镀池中电极反应的书写和阴阳极材料的判断,应注意镀层材料做阳极.


科目:高中化学 来源: 题型:解答题
 ,天然硼元素有两种稳定同位素10B、11B,其相对原子质量分别为10和11,它们的相对丰度分别为20%和80%,硼元素的平均相对质量为10.8.
,天然硼元素有两种稳定同位素10B、11B,其相对原子质量分别为10和11,它们的相对丰度分别为20%和80%,硼元素的平均相对质量为10.8.| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 2.7 | 5.0 | 8.7 | 14.8 | 23.8 |
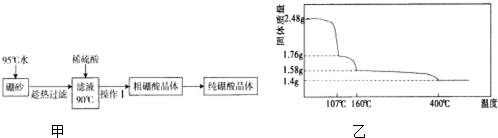
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W | ||
| T |
| A. | X、Y、Z三种元素最低价氢化物的沸点依次升高 | |
| B. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| C. | 含Z元素的弱酸不能与含W元素的弱酸反应得到强酸 | |
| D. | T元素形成的酸与W元素形成的酸相比,酸性一定后者弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用活性炭去除汽车内室的异味 | |
| B. | 用硝酸对钢船舱进行钝化处理 | |
| C. | 用经硫酸酸化处理的三氧化铬硅胶检验酒精 | |
| D. | 用小苏打溶水拌入面中一起蒸煮使馒头蓬松 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氨是重要的化工原料,用途很广.
氨是重要的化工原料,用途很广.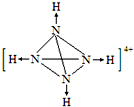 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “雨后彩虹”是一种与光学和胶体性质相关的自然现象 | |
| B. | 纯银器表面在空气渐渐变暗,是电化学腐蚀所致 | |
| C. | 右图电流表指针偏转,有电流通过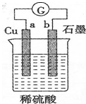 | |
| D. | 在食品中科学使用食品添加剂对人体无害 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
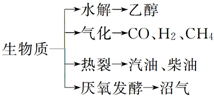 “地沟油”被称为“生物燃料”,该燃料属于生物质能.已知生物质的主要转化途径及主要产物如图所示.则下列关于生物燃料以及生物质能的说法中正确的是( )
“地沟油”被称为“生物燃料”,该燃料属于生物质能.已知生物质的主要转化途径及主要产物如图所示.则下列关于生物燃料以及生物质能的说法中正确的是( )| A. | ①②③④⑤ | B. | ①②④⑤ | C. | ③④⑤ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com