
下列关于物质分类的说法正确的是( )
A. 化合反应均为氧化还原反应
B. 液氨、液氯、液体氯化氢都是非电解质
C. 多糖、油脂、蛋白质都是高分子化合物
D. 古代的陶瓷、砖瓦,现代的玻璃、水泥等,都是硅酸盐产品
科目:高中化学 来源: 题型:
向体积为0.05mol·L-1CH3COOH溶液中加入体积为Vb的0.05mol·L-1KOH溶液,下列关系错误的是
A. Va>Vb时:c (CH3COOH) +c (CH3COO-)>c (K+)
B. Va=Vb时:c (CH3COOH) +c (H+)>c (OH-)
C. Va<Vb时:c (CH3COO-)>c (K+)> c (OH-)> c (H)
D. Va与Vb任意比时:c (K+)+ c (H+) =c (OH-)+ c (CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是 ( )
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+m,则X的最高正价一定为+m
查看答案和解析>>
科目:高中化学 来源: 题型:
反应2H2S(g)  2H2(g)+S2(g) ΔH >0,其他条件不变,下列说法正确的是
2H2(g)+S2(g) ΔH >0,其他条件不变,下列说法正确的是
A.加入催化剂,反应路径将发生改变,ΔH也将随之改变
B.升高温度,正逆反应速率都增大,H2S分解率也增大
C.增大压强,平衡向逆反应方向移动,体系温度降低
D.恒容体系,充入H2重新达到平衡后,H2浓度将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
I.在温度为T时,向2.0 L恒容密闭容器中充入1.0 mol A和1.0 mol B,发生反应A(g)+B(g)  C(g),一段时间后达到平衡。测定得部分数据见下表:
C(g),一段时间后达到平衡。测定得部分数据见下表:
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
回答下列问题:
(1)反应前5 s的平均反应速率v(A) =____________
(2)温度为T时,该反应的化学平衡常数=
(3)升高温度,平衡时c(A)=0.41 mol·L-1,则反应的ΔH (填 “>0” 或 “<0”)
(4)相同温度下,起始时向容器中充入0.2 mol A、0.2 mol B和1.0 mol C,反应达到平衡前,反应速率v正 v逆(填“>” 或 “<”)
(5)下列措施能增大反应速率,且平衡往正反应方向移动是 。
a.及时分离出A气体 b.适当升高温度
c.增大B的浓度 d.选择高效催化剂
II.NO、NO2是常见的氧化物。用H2或CO催化还原NO可达到消除污染的目的。
已知:2NO(g) = N2(g) + O2(g) △H = -180.5kJ·mol-1
2H2O(l) = 2H2(g) + O2(g) △H = +571.6kJ·mol-1
则用H2催化还原NO消除污染的热化学方程式是
查看答案和解析>>
科目:高中化学 来源: 题型:
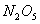 是一种新型硝化剂,在一定温度下可发生以下反应:
是一种新型硝化剂,在一定温度下可发生以下反应:
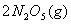

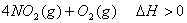
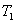 温度时,向密闭容器中通入
温度时,向密闭容器中通入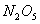 ,部分实验数据见下表:
,部分实验数据见下表:
|
| 0 | 500 | 1000 | 1500 |
|
| 5.00 | 3.52 | 2.50 | 2.50 |
下列说法中不正确的是( )
A. 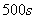 内
内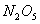 分解速率为
分解速率为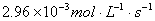
B. 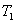 温度下的平衡常数
温度下的平衡常数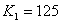 ,平衡时
,平衡时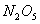 的转化率为50%
的转化率为50%
C. 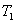 温度下的平衡常数为
温度下的平衡常数为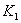 ,
,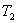 温度下的平衡常数为
温度下的平衡常数为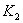 ,若
,若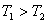 ,则
,则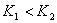
D. 达平衡后其他条件不变,将容器的体积压缩到原来的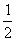 ,则再次平衡时
,则再次平衡时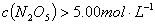
查看答案和解析>>
科目:高中化学 来源: 题型:
把下列四种X溶液分别加入四个盛有10mL 2mol/L盐酸的烧杯中,均加水稀释到50mL,此时,X和盐酸缓慢地进行反应,其中反应最快的是( )
A.10℃20mL 3mol/L的X溶液 B.20℃30mL 2mol/L的X溶液
C.20℃10mL 4mol/L的X溶液 D.10℃10mL 2mol/L的X溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
500m L KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
①原混合溶液中c(K+)= 4mol·L-1 ②原混合溶液中c(K+)= 2mol·L-1
③电解得到的Cu的物质的量为0.5mol ④电解后溶液中c(H+)=2mol·L-1
⑤向电解后的溶液中加入一定量的CuO可恢复为原溶液
⑥向电解后的溶液中加入一定量的Cu(OH)2可恢复为原溶液
⑦上述电解过程中共转移了4mol电子 ⑧电解后溶液中c(H+)=4mol·L-1
A.②⑥⑦⑧ B.①④⑤⑦ C.②⑤⑦⑧ D.①③④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com