
| A. | 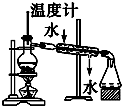 用图分离两种互溶但沸点相差较大的液体混合物 | |
| B. | 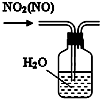 用图所示装置可除去NO2中的NO | |
| C. | 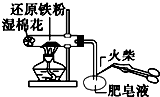 用图检验铁粉与水蒸气反应产生的氢气 | |
| D. | 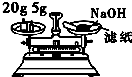 用图称量氢氧化钠固体 |
分析 A.分离两种互溶但沸点相差较大的液体混合物,选择蒸馏法,温度计测定馏分的温度,冷却水应下进上出;
B.二氧化氮与水反应;
C.Fe与水蒸气高温下反应生成氢气,氢气具有可燃性;
D.称量固体左物右码,且NaOH具有腐蚀性.
解答 解:A.分离两种互溶但沸点相差较大的液体混合物,选择蒸馏法,温度计测定馏分的温度,冷却水应下进上出,图中冷却水的方向不合理,故A错误;
B.二氧化氮与水反应,将原物质除去,不符合除杂的原则,故B错误;
C.Fe与水蒸气高温下反应生成氢气,氢气具有可燃性,点燃肥皂泡可验证氢气的生成,故C正确;
D.称量固体左物右码,且NaOH具有腐蚀性,则NaOH应在左盘且放在小烧杯中称量,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、物质的性质、实验基本操作等,把握物质的性质、实验技能为解答的关键,侧重分析与实验能力的综合考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 放热反应在常温下一定很容易发生 | |
| B. | 化学反应一定既伴随着物质变化又伴随着能量变化 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 反应物所具有的总能量高于生成物所具有的总能量的反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的氢化物溶于水显酸性且稳定性弱于HF | |
| B. | Y的氧化物是离子化合物,Y的氢氧化物碱性比氢氧化钠弱 | |
| C. | Z的氢化物的水溶液在空气中存放不易变质 | |
| D. | X和Z的最高价氧化物对应的水化物都是弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④⑤③ | B. | ⑥①⑤③ | C. | ③⑤①② | D. | ⑥① |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
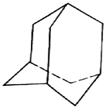 有的油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示:
有的油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCN 与KOCN中氮元素的化合价均为-3价 | |
| B. | 氰酸盐进一步被氧化的产物之一是无毒的N2 | |
| C. | OCN-与CN-中σ键与π键个数比均为1:2 | |
| D. | 完全处理含0.1 mol CN-的废水,理论上需要消耗Cl2的体积为5.6L(标准状况下) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法不正确的是( )
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法不正确的是( )| A. | 对应简单离子半径②>⑧>⑨ | |
| B. | 简单氢化物稳定性⑤>⑧ | |
| C. | 最高价氧化物对应的水化物酸性⑨>⑧>⑦ | |
| D. | ①分别与③、④、⑤均可形成既含极性键又含非极性键的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌为正极,空气进入负极反应 | B. | 负极反应为:Zn-2e-=Zn2+ | ||
| C. | 正极发生氧化反应 | D. | 正极反应为:Zn-2e-=Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| B. | 在上述条件下,SO2不可能100%地转化为SO3 | |
| C. | 无论怎样控制反应条件,2 mol SO2与1 mol O2 反应时都不会生成2 mol SO3 | |
| D. | 达到平衡时,SO2的浓度与SO3的浓度相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com