
| A. | 温度越高,酶的催化活性越强 | |
| B. | 浓硝酸使皮肤呈黄色是由于浓硝酸与蛋白质发生了显色反应 | |
| C. | 用灼烧的方法可以鉴别毛织物和棉织物 | |
| D. | 在豆浆中加入少量的石膏,能使豆浆凝结为豆腐 |
分析 A.高温能使蛋白质发生变性;
B.含苯环的蛋白质遇浓硝酸发生颜色反应;
C.毛织物的成分为蛋白质,灼烧有烧焦羽毛的气味;
D.豆浆中加入少量的石膏,发生胶体的聚沉.
解答 解:A.高温能使蛋白质发生变性,则应在合适的温度下酶的催化活性最强,故A错误;
B.含苯环的蛋白质遇浓硝酸发生颜色反应,则浓硝酸使皮肤呈黄色是由于浓硝酸与蛋白质发生了显色反应,故B正确;
C.毛织物的成分为蛋白质,灼烧有烧焦羽毛的气味,则用灼烧的方法可以鉴别,故C正确;
D.豆浆中加入少量的石膏,发生胶体的聚沉,能使豆浆凝结为豆腐,故D正确;
故选A.
点评 本题考查物质的鉴别和检验,为高频考点,把握有机物的结构与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机反应的应用,题目难度中等.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:选择题
| A. | 只有②④ | B. | 只有①③ | C. | 只有①②③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ④CH3COOH⑤HOCH2CHO ⑥CH3CH2CH2CH3⑦葡萄糖 ⑧蛋白质⑨淀粉
④CH3COOH⑤HOCH2CHO ⑥CH3CH2CH2CH3⑦葡萄糖 ⑧蛋白质⑨淀粉查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
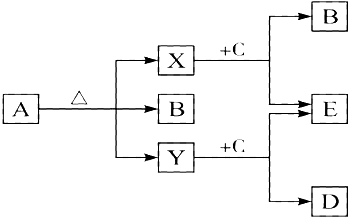
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
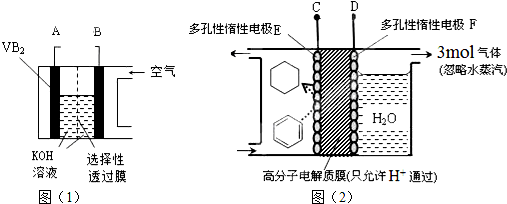
| A. | 整套装置工作时的连接为A连接D、B连接C | |
| B. | VB2极发生的电极反应为:2VB2+22OH--22e-═V2O5+2B2O3+11H2O | |
| C. | 电极F产生3mol气体时电极E得到的氧化产物为2mol | |
| D. | 储氢装置工作时,右侧电极区的pH值减小2×10-9 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
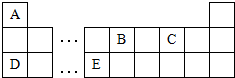
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com