
己知Ksp(AgCl)=1.56×10-10、Ksp(AgBr)=7.7×10-13、Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有C1--, Br--和CrO42--浓度均为0.010mo1/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( )
A. C1--、Br--、CrO42-- B. CrO42--、Br--、C1--
C. Br--、C1--、CrO42-- D. Br-- 、CrO42--、C1--
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
把1.1 g铁、铝混合物溶于200 mL 5 mol·L-1盐酸中,反应后盐酸的浓度变为4.6 mol·L-1(溶液体积变化忽略不计)。求:
(1)反应中消耗HCl的物质的量。
(2)该混合物中铝、铁的物质的量。
查看答案和解析>>
科目:高中化学 来源: 题型:
有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有白色沉淀产生。
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99 g。
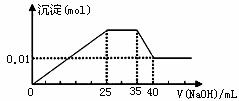
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图。根据上述实验,以下推测不正确的是
A.原溶液一定不存在H+、Cu2+、CO32-
B.不能确定原溶液是否含有K+、NO3-
C. 实验所加的NaOH的浓度为2mol·L-1
D. 原溶液确定含Mg2+、Al3+、NH4+,且n(Mg2+)n(Al3+)n( NH4+)=112
查看答案和解析>>
科目:高中化学 来源: 题型:
用NaOH滴定pH相同、体积相同的H2SO4、HCl、CH3COOH三种溶液,恰好中和时,所用相同浓度NaOH溶液的体积依次为V1、V2、V3,则这三者的关系是( )
A.V1>V2>V3 B.V1<V2<V3 C.V1=V2>V3 D.V1=V2<V3
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:25°C时,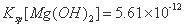 ,
,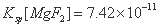 。下列说法正确的是
。下列说法正确的是
A.25°C时,饱和 溶液与饱和
溶液与饱和 溶液相比,前者的
溶液相比,前者的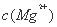 大
大
B.25°C时,在 的悬浊液中加入少量的
的悬浊液中加入少量的 固体,
固体,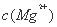 增大
增大
C.25°C时, 固体在20ml0.01 mol·
固体在20ml0.01 mol· 氨水中的Ksp比在20mL 0.01mol·
氨水中的Ksp比在20mL 0.01mol·
 溶液中的Ksp小
溶液中的Ksp小
D.25°C时,在 的悬浊液中加入NaF溶液后,不可能有
的悬浊液中加入NaF溶液后,不可能有 生成
生成
查看答案和解析>>
科目:高中化学 来源: 题型:
I.某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
A.在天平上准确称取烧碱样品Wg,在烧杯中加蒸馏水溶解
B.在250mL容量瓶中定容成250mL烧碱溶液
C.用碱式滴定管移取25mL烧碱溶液于锥形瓶中并滴加几滴酚酞
D.将物质的量浓度为M mol/L的标准盐酸装入酸式滴定管,调整液面,记下开始刻度为V1 mL。
E.锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
回答下列问题:
(1)滴定达到终点的现象是 ;
(2)若酸式滴定管没有用标准盐酸润洗,会对测定结果有何影响 (填“偏高”“偏低”或“无影响”,其它操作均正确)
(3)该烧碱样品的纯度计算式是 。
II.(4)任何一个自发的氧化还原反应都可以设计成一个原电池。请根据:Fe+2Fe3+=3Fe2+,设计成一个原电池。该电池的正极材料为_____,其电极反应为__________________;电池中的电解质溶液可以选择 。
查看答案和解析>>
科目:高中化学 来源: 题型:
随着人们生活质量提高,废电池必须进行集中处理的问题又被提到议事日程上,其首要原因是( )
A.利用电池外壳的金属材料
B.回收其中石墨电极
C.防止电池中汞、镉和铅等重金属离子对水和土壤的污染
D.不使电池中泄漏的电解液腐蚀其他物品
查看答案和解析>>
科目:高中化学 来源: 题型:
大气中的臭氧层可使人类和其他生物免受紫外线的危害,人为因素可能使臭氧层受到破坏,下列因素可破坏臭氧层的是( )
A.SO2的排放
B.制冷剂氟氯烃(商品名氟利昂)的泄漏
C.CO2的排放
D.燃料的不完全燃烧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com