
【题目】除去括号内杂质所用试剂和方法均正确的是
A.乙酸乙酯(乙酸):饱和碳酸钠溶液、分液
B.苯(环己烯):溴水、分液
C.苯(苯酚):溴水、过滤
D.乙烷(乙烯):酸性高锰酸钾溶液、洗气
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】水合肼(N2H4·H2O)是无色、有强还原性的液体,实验室制备水合肼的原理为:
CO(NH2)2+2NaOH+NaClO==Na2CO3+N2H4·H2O+NaCl
据此,某学生设计了下列实验.
【制备NaClO溶液】实验装置如下图左图所示(部分夹持装置已省略)
已知:3NaClO![]() 2NaCl+NaClO3
2NaCl+NaClO3
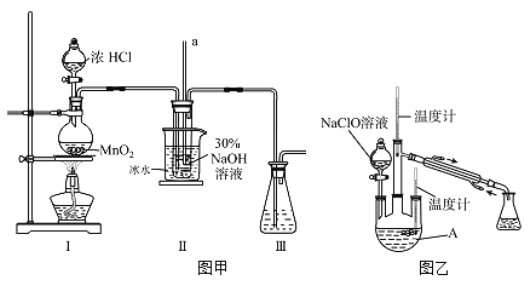
(1)配制30 %NaOH溶液时,所需玻璃仪器除量筒外还有__________(填字母)。
A.容量瓶 B.烧杯 C.移液管 D.玻璃棒
(2)装置I中发生的离子反应方程式是_______________;Ⅱ中玻璃管a的作用为____________;为了提高NaClO的产率,需对I中产生的Cl2进行净化,所用试剂是________________;Ⅱ中用冰水浴控制温度在30℃以下,其主要目的___________________
【制取水合肼】实验装置如上图右图所示
(3)反应过程中,如果分液漏斗中溶液的滴速过快, 部分N2 H4·H2O参与A中反应并产生大量氮气,产品产率因此降低,请写出降低产率的相关化学反应方程式____________________;充分反应后,加热蒸馏A内的溶液即可得到水合肼的粗产品,B装置的名称是______________
【测定肼的含量】
(4)称取馏分0.3000 g,加水配成20.0 mL溶液,一定条件下用0.1500 mol.L-1 的I2溶液滴定。
已知: N2H4·H2O + 2I2 = N2↑+ 4HI + H2O。
①滴定时,可以选用的指示剂为____________;
②实验测得消耗I2溶液的平均值为20. 00 mL,馏分中N2H4·H2O的质量分数为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是
A.乙烯水化制乙醇;溴乙烷水解制乙醇
B.由乙醇制乙烯;溴乙烷与氢氧化钠醇溶液共热制乙烯
C.苯硝化制硝基苯;乙烯使酸性高锰酸钾溶液褪色
D.甲苯使酸性高锰酸钾溶液褪色;丙炔使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯过氧化氢是淡蓝色的黏稠液体,可与水以任意比混合,其水溶液俗称双氧水,为无色透明液体。实验室常用过氧化氢制取氧气,工业上过氧化氢是重要的氧化剂和还原剂,常用于消毒、杀菌、漂白等。某化学兴趣小组的同学围绕过氧化氢开展了调查研究与实验,请你参与其中一起完成下列学习任务:
(1)写出过氧化氢的电子式:________。
(2)实验室中用过氧化氢制取氧气的化学方程式为_______________,当生成标准状况下1.12 L O2时,转移电子为________ mol。
(3)该兴趣小组的同学查阅资料后发现H2O2为二元弱酸,其酸性比碳酸弱。请写出H2O2在水溶液中的电离方程式:______________________。
(4)同学们用0.1000 mol·L-1的酸性高锰酸钾标准溶液滴定某试样中过氧化氢的含量,反应原理为2MnO4-+5H2O2+6H+===2Mn2++8H2O+5O2↑。
①在该反应中,H2O2被________(填“氧化”或“还原”)。
②滴定到达终点的现象是______________________________________。
③用移液管吸取25.00 mL试样置于锥形瓶中,重复滴定四次,每次消耗的酸性KMnO4标准溶液体积如下表所示:
第一次 | 第二次 | 第三次 | 第四次 | |
体积(mL) | 17.10 | 18.10 | 17.00 | 16.90 |
则试样中过氧化氢的浓度为________mol·L-1。
④若滴定前尖嘴中有气泡,滴定后消失,则测定结果____(填“偏低”、“偏高”或“不变”)。
(5)同学们发现向滴加了酚酞的NaOH溶液中加入H2O2后,溶液中红色消失。关于褪色原因:甲同学认为H2O2是二元弱酸,消耗了OH-使红色消失;乙同学认为H2O2具有漂白性使溶液褪色。请设计一个简单的实验方案来判断甲、乙两位同学的说法是否正确_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关组成生物体细胞的化学元素的叙述,错误的是
A. 构成细胞的最基本元素是碳
B. H7N9病毒和桃树共有的元素是C、H、0、N、P等
C. 生物体内含有的元素都是生物体所必需的
D. Cu、Mn、Mo、B都是组成生物体的微量元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,需加氧化剂才能实现的是
A. Cl2 →NaClO B. H2O2 → O2 C. (NH4)2SO4 →N2 D. CaO→CaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列混合物的物质的量一定时,组内各物质按任意比混合,完全燃烧时耗O2的量不变的是
A. 甲烷、甲醇、甲醛 B. 丙烯酸(CH2=CH-COOH)、乙烯、乙醇
C. 丙烯、2-丁烯、环已烷 D. 乙炔、苯、1,3-丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室安卡因(G)是一种抗心律失常药物,可由下列路线合成:
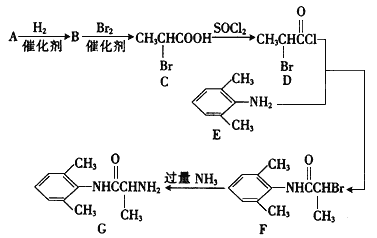
I.(1)己知A是 的单体,则A中所含官能团的名称是____________。
的单体,则A中所含官能团的名称是____________。
(2)写出B的结构简式并用系统命名法给C命名: B:_____________, C的名称:____________。
(3)L是E的同分异构体,L分子中含有苯环,且苯环上一氯代物只有两种,则L所有可能的结构简式有![]() 、__________________。
、__________________。
(4)F →G的反应类型是_______________。
(5)下列关于室安卡因(G)的说法正确的是____________。
a.能发生加成反应 b.能使酸性高锰酸钾溶液褪色
c.能与盐酸反应生成盐 d.属于氨基酸
(6)写出C与足量NaOH醇溶液共热时反应的化学方程式:______________。
II. H是C的同系物,其核磁共振氢谱有两个峰。按如下路线,由H可合成高聚物V:
![]()
(7)H的结构简式为_________________;N→Q的反应类型为________________。
(8)写出Q→V的反应方程式:________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com