
| A. | 工业制备NaClO可用电解饱和食盐水的方法离子方程式为:Cl-+H2O $\frac{\underline{\;电解\;}}{\;}$ ClO-+H2↑ | |
| B. | 向NaClO溶液中通入少量SO2气体离子方程式为:SO2+3ClO-+2H2O═2HClO+SO42-+Cl- | |
| C. | 在NaClO溶液中可以大量共存的离子有:K+,SO42-,Fe3+,NO3- | |
| D. | 84消毒液不能和洁厕剂混合使用,也不能用pH试纸测其pH值. |
分析 A.电解饱和食盐水生成NaOH、氢气、氯气;
B.发生氧化还原反应生成硫酸根离子;
C.该组离子之间均不反应;
D.NaClO与盐酸发生氧化还原反应生成氯气,且NaClO溶液具有漂白性.
解答 解:A.电解饱和食盐水生成NaOH、氢气、氯气,发生2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$ 2OH-+H2↑+Cl2↑,故A错误;
B.发生氧化还原反应生成硫酸根离子,离子反应为SO2+3ClO-+2H2O═2HClO+SO42-+Cl-,故B正确;
C.该组离子之间均不反应,可大量共存,故C正确;
D.NaClO与盐酸发生氧化还原反应生成氯气,则84消毒液不能和洁厕剂混合使用,且NaClO溶液具有漂白性,可知不能用pH试纸测其pH值,故D正确;
故选A.
点评 本题考查离子反应方程式及离子共存,为高频考点,把握物质的性质及发生的离子反应为解答本题的关键,注意发生的氧化还原反应中电子、电荷守恒及NaClO的性质,题目难度不大.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
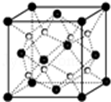 原子序数依次递增且都小于36的X、Y、Z、Q、W四种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Q原子基态时2p原子轨道上有2个未成对的电子,W元素的原子结构中3d能级有4个未成对电子.回答下列问题:
原子序数依次递增且都小于36的X、Y、Z、Q、W四种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Q原子基态时2p原子轨道上有2个未成对的电子,W元素的原子结构中3d能级有4个未成对电子.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液呈浅绿色 | |
| B. | 该溶液中加入NaOH溶液,生成白色沉淀并迅速变成灰绿色,最终变为红褐色 | |
| C. | 向该溶液中加入氯水,再滴入几滴KSCN溶液,呈红色 | |
| D. | 向该溶液中滴入几滴KSCN溶液,不变色,再加入氯水,有红色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某种食品的配料标签如图所示.
某种食品的配料标签如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8 g Na2O2与足量水反应转移的电子数为0.2NA | |
| B. | 常温常压下,1 mol CH4中含有的氢原子数为4NA | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA | |
| D. | 12.0 g熔融的NaHSO4中含有0.1NA个Na+、0.1NA个H+和0.1NA个SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 互为同分异构体 | B. | 互为同系物 | C. | 只能是同种物质 | D. | 最简式一定相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com