
已知一定条件下合成氨反应:N2(g)+3H2(g)2NH3(g) ΔH=-92.4 kJ·mol-1,在反应过程中,反应速率的变化如图所示,请根据速率的变化回答采取的措施。
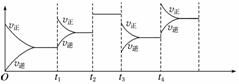
t1____________;t2______________;t3______________;
t4____________。
科目:高中化学 来源: 题型:
已知某油脂A,在硫酸作催化剂的条件下水解,生成脂肪酸和多元醇B,B和硝酸通过酯化反应生成有机物D。
(1)写出油脂A在硫酸作催化剂的条件下水解的化学方程式:________________________________________________________________________。
(2)已知D的相对分子质量为227,由C、H、O、N四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%。则D的分子式是________,写出B→D的化学方程式:________________________________________________________________________。
(3)C是由B和乙酸在一定条件下反应生成的化合物,相对分子质量为134,写出C所有可能的结构简式________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1∶1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为____________;b的化学式为______________;c的电子式为________;d的晶体类型是______。
(4)由A和B、D元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过________键构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )。
A.用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl--2e-===Cl2↑
B.氢氧燃料电池的负极反应式:O2+2H2O+4e-===4OH-
C.粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu-2e-===Cu2+
D.钢铁发生电化学腐蚀的正极反应式:Fe-2e-===Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组同学设想用如图装置电解硫酸钾溶液来
制取氧气、氢气、硫酸和氢氧化钾。
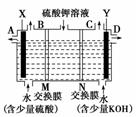
(1)X极与电源的________(填“正”或“负”)极相连,氢气从________(选填“A”、“B”、“C”或“D”)口导出。
(2)离子交换膜只允许一类离子通过,则M为________(填“阴离子”或“阳离子”,下同)交换膜,N为________交换膜。
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为________________________________________________________
________________________________________________________________________。
(4)若在标准状况下,制得11.2 L氢气,则生成硫酸的质量是________,转移的电子数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在等温等容条件下,可逆反应:2A(g)+B(g)3C(g)+D(g) ΔH=-Q1 kJ·mol-1(Q1>0),起始物质的量如下表所示:
| 序号 | A | B | C | D |
| ① | 2 mol | 1 mol | 0 | 0 |
| ② | 4 mol | 2 mol | 0 | 0 |
| ③ | 1 mol | 0.5 mol | 1.5 mol | 0.5 mol |
| ④ | 0 | 1 mol | 3 mol | 1 mol |
| ⑤ | 0 | 0 | 3 mol | 1 mol |
(1)上述反应达到平衡时,互为等效平衡的是哪几组?达到平衡后,哪些量相同?
(2)达到平衡后,①放出的热量为Q2 kJ,⑤吸收的热量为Q3 kJ,则Q1、Q2、Q3的定量关系为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒容密闭容器中通入X并发生反应:2X(g)Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示。下列叙述正确的是( )
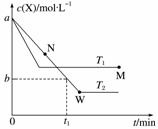
A.该反应进行到M点放出的热量大于进行到W点放出的热量
B.T2下,在0~t1时间内,v(Y)= mol·L-1·min-1
C.M点的正反应速率v正大于N点的逆反应速率v逆
D.M点时再加入一定量X,平衡后X的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,容积相同的甲、乙、丙3个恒容密闭容器中均发生如下反应:2SO2(g)+O2(g)2SO3(g) ΔH=-197 kJ·mol-1,实验测得有关数据如下:
| 容器编号 | 起始时各物质的物质的量 /mol | 达到平衡时体系能量的变化数值 /kJ | ||
| SO2 | O2 | SO3 | ||
| 甲 | 2 | 1 | 0 | Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | Q2 |
| 丙 | 0 | 0 | 2 | Q3 |
下列判断中正确的是( )
A.197>Q2>Q1
B.若升高温度,反应的热效应不变
C.Q3=197
D.生成1 mol SO3(l)时放出的热量大于98.5 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
在常压和500 ℃条件下,等物质的量的Ag2O、Fe(OH)3、NH4HCO3、NaHCO3,完全分解,所得气体体积依次为V1、V2、V3、V4。体积大小顺序正确的是( )
A.V3>V2>V4>V1 B.V3>V4>V2>V1
C.V3>V2>V1>V4 D.V2>V3>V1>V4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com