
| �¶�/�� | 1000 | 1150 | 1300 |
| ƽ�ⳣ�� | 42.9 | 50.7 | 64.0 |
���� ��1��KΪ������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ��ɱ������ݿ�֪���¶�Խ�ߣ�KԽ��
��2��1300��ʱK=64����Ӧ����10min ��ﵽƽ�⣬Qc=1��K��ƽ�������ƶ�����ת����COΪx����
Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g��
��ʼ 1 1
ת�� x x
ƽ�� 1-x 1+x
��֪$\frac{��1+x��^{3}}{��1-x��^{3}}$=64�����x=0.6��
��3����ߣ�2����CO��ƽ��ת���ʣ�Ӧʹƽ�������ƶ��������ܼ�CO���Դ������
��� �⣺��1��Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g�� ��K=$\frac{{c}^{3}��C{O}_{2}��}{{c}^{3}��CO��}$���ɱ������ݿ�֪���¶�Խ�ߣ�KԽ������ӦΪ���ȷ�Ӧ����H��0��
�ʴ�Ϊ��$\frac{{c}^{3}��C{O}_{2}��}{{c}^{3}��CO��}$������
��2��1300��ʱK=64����Ӧ����10min ��ﵽƽ�⣬Qc=1��K��ƽ�������ƶ�����ת����COΪx����
Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g��
��ʼ 1 1
ת�� x x
ƽ�� 1-x 1+x
��֪$\frac{��1+x��^{3}}{��1-x��^{3}}$=64�����x=0.6��
v��CO2��=$\frac{\frac{0.6mol}{10L}}{10min}$=0.006mol/��L•min����
CO ��ƽ��ת����Ϊ$\frac{0.6}{1}$��100%=60%��
�ʴ�Ϊ��0.006mol/��L•min����60%��
��3��A������Fe2O3������ƽ�ⲻ�ƶ�����A��ѡ��
B��������ʵĴ�����ƽ�ⲻ�ƶ�����B��ѡ��
C���Ƴ�����CO2��ƽ�������ƶ���CO��ת��������Cѡ��
D���÷�ӦΪ���ȷ�Ӧ����߷�Ӧ�¶ȣ�ƽ�������ƶ���CO��ת��������Dѡ��
�ʴ�Ϊ��CD��
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ��Ƶ���㣬����ƽ�����η���K��ת���ʺ����ʵļ��㡢ƽ���ƶ�Ϊ���Ĺؼ������ط�������������Ŀ��飬ע��K��Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ѱ���Ũ��ˮ��Ϻ����FeBr3�����屽 | |
| B�� | Ũ������Ũ��������ȴ�ߵ��뱽������60��ˮԡ�м��ȿ��������� | |
| C�� | �����л�����ϩ��ͨ����������ϩ��Ӧ�ɴﵽ���ӵ�Ŀ�� | |
| D�� | ��ϩͨ��ˮ�п��Ƶþƾ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ���������������� | B�� | һ�������������ı仯 | ||
| C�� | ���ܻ���������״̬�ı仯 | D�� | �л�ѧ���ƻ���һ���ǻ�ѧ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���� | B�� | �Ĵ� | C�� | �崦 | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
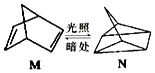 ��̼�Ļ�����֮���������ת������ش��������⣺
��̼�Ļ�����֮���������ת������ش��������⣺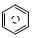 ��l����ȼ����Ϊ 3267.5kJ•mol-1��
��l����ȼ����Ϊ 3267.5kJ•mol-1��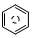 ��l��+6O 2��g���T6CO2 ��g��+3H2 ��g��
��l��+6O 2��g���T6CO2 ��g��+3H2 ��g���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
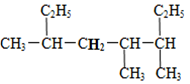
| A�� | 4��5-����-2-�һ����� | B�� | 3��4-����-6-�һ����� | ||
| C�� | 4-��-2��5-���һ����� | D�� | 3��4��6-�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡH2SO4��HCl����AgNO3��Һ������ | B�� | KNO3��K2SO4����Ba��NO3��2��Һ������ | ||
| C�� | Cu��CuO�������ᡢ���� | D�� | CaCO3��CaO�������ᡢ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �ù��˵ķ���������������������Ȼ�����Һ | |
| B�� | ��������ȡ��ˮ�е��� | |
| C�� | ���ܽ⡢���˵ķ����ᴿ�����������ᱵ��̼��� | |
| D�� | �÷�Һ�ɷ��������������Ҵ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com