
【题目】下列说法正确的是
①正常雨水的pH为7.0,酸雨的pH小于7.0;
②严格执行机动车尾气排放标准有利于防止大气污染;
③使用二氧化硫和某些含硫化合物增白的食品会损害人体健康;
④使用氯气对自来水消毒可能对人体有害;
⑤食品厂产生的含丰富氮、磷营养素的废水可长期排向养鱼水库
A. ①②③ B. ①④⑤ C. ②③④ D. ③④⑤
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为Ts(中文名“ ![]() ”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )
”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )
A. Ts是第七周期第ⅦA族元素 B. Ts的同位素原子具有相同的电子数
C. Ts在同族元素中非金属性最弱 D. 中子数为176的TS核素符号是 ![]() Ts
Ts
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在Ni基催化剂作用下,CH4和CO2反应可获得化工原料CO和H2。基态Ni原子的外围电子排布式为 ,该元素位于元素周期表中的第 族。
(2)碳元素能够形成不同的单质,如C60、C70、金刚石等等。
①C60、C70、金刚石这些单质间互称为 。
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C60分子的个数比为 。

③继C60后,科学家又合成了Si60、N60, C、Si、N三种原子电负性由大到小的顺序是 。
(3)铜单质及其化合物在很多领域有重要用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
①Cu位于元素周期表第ⅠB族。Cu2+的核外电子排布式为 。
②Cu2O的熔点比Cu2S的 (填“高”或“低”),请解释原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1molCO和2molH2充入密闭容器中,发生反应:CO(g)+2H2(g)![]() CH3OH(g) △H。在其他条件相同时,测得CO平衡转化率[α(CO)]与温度和压强的关系如下图。
CH3OH(g) △H。在其他条件相同时,测得CO平衡转化率[α(CO)]与温度和压强的关系如下图。
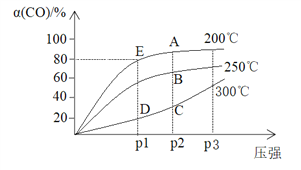
下列说法不正确的是
A. △H <0
B. C、D两点的反应速率:v(C)> v(D)
C. 若E点的容器体积为10L,该温度下的平衡常数为k=25
D. 工业生产中实际控制的条件200℃、P2压强,不采用P3的理由是,增大压强转化率变化不大,而且工业成本调高,得不偿失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)0.5 mol CO2 的质量为_____克,其中含有 CO2 分子_____个,在标准状况下的体积是_____升。
(2)标况下,1.92 g 某气体的体积为 672 mL,则此气体的相对分子质量为_____。
(3)已知某硫酸溶液的密度为 1.84 g/cm3,质量分数为 98%,则该硫酸的物质的量浓度为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项正确的是( )
A. 镁、铝与沸水不可能反应
B. 铁在一定条件下可以与水反应
C. 钠与水反应的离子方程式:Na+H2O=Na++OH-+H2↑
D. 钠和硫酸铜溶液反应的离子方程式:2Na+Cu2+=2Na++Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,将10mL某气态烃,在60mLO2里充分燃烧,得到液态水和体积为45mL的混合气体,则该烃可能为( )
A.甲烷B.乙烷C.丙烷D.乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组按下列路线合成镇痛药哌替啶:
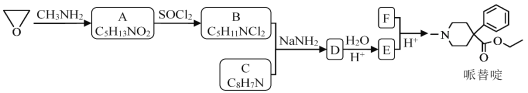
已知: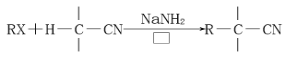
请回答:
(1)A→B的反应类型是________。
(2)下列说法不正确的是________(填字母)。
A.化合物A的官能团是硝基 B.化合物B可发生消去反应
C.化合物E能发生加成反应 D.哌替啶的分子式是C15H21NO2
(3)写出B+C→D的化学反应方程式________。
(4)设计以甲苯为原料制备C的合成路线__________________(用流程图表示,无机试剂任选)。
(5)写出同时符合下列条件的C的所有同分异构体的结构简式________。
①分子中有苯环而且是苯环的邻位二取代物;
②1HNMR谱表明分子中有6种氢原子;IR谱显示存在碳氮双键(C=N)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是
A. 32 g O2和O3的混合气体所含原子数为NA
B. 5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA
C. 高温下,0.2mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
D. 在25℃、101kPa下,2 mol氧气和氢气的混合气体的体积约为44.8 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com