
分析 (1)可逆反应到达平衡时,同种物质的正逆速率相等且保持不变,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化说明到达平衡;
(2)已知:①CO(g)+2H2(g)=CH3OH(g)△H1=-100.46kJ/mol
②2CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H=-204.7kJ/mol
根据盖斯定律:②-①×2得:2CH3OH(g)=CH3OCH3(g)+H2O(g);
(3)硝酸铝与Na2CO3水溶液发生相互促进的水解反应生成氢氧化铝沉淀和二氧化碳气体;
(4)该燃料电池中,氧气在正极得电子,负极上二甲醚失电子发生氧化反应生成二氧化碳
解答 解:(1)A.CO和H2的物质的量浓度比与反应物的初始量及转化率有关,所以不能说明到达平衡状态,故A错误;
B.CO的消耗速率与CH3OCH3的生成速率都属于正速率,速率之比等于计量数之比,始终为高比例关系,不能说明到达平衡状态,故B错误;
C.随反应进行混合气体总物质的量减少,由于压强不变,则气体的体积会减小,容器中混合气体的体积保持不变,说明到达平衡状态,故C正确;
D.气体的总质量保持不变,气体总物质的量减少,则气体的平均摩尔质量逐渐增大,当容器中混合气体的平均摩尔质量保持不变,说明到达平衡状态,故D正确;
E.气体的总质量保持不变,气体的体积减小,则密度增大,当容器中混合气体的密度保持不变,说明反应到达平衡状态,故E正确;
故答案为:CDE;
(2)已知:①CO(g)+2H2(g)=CH3OH(g)△H1=-100.46kJ/mol
②2CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H=-204.7kJ/mol
根据盖斯定律:②-①×2得:2CH3OH(g)=CH3OCH3(g)+H2O(g)△H2=-204.7kJ/mol-(-100.46kJ/mol)×2=-3.78kJ/mol;
故答案为:-3.78kJ/mol;
(3)硝酸铝与Na2CO3水溶液发生相互促进的水解反应生成氢氧化铝沉淀和二氧化碳气体,其水解的离子方程式为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑,
故答案为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑.
(4)该燃料电池中,氧气在正极得电子,则通入氧气的电极是电源的正极,负极上二甲醚失电子发生氧化反应生成二氧化碳,则负极反应式为:CH3OCH3+3H2O-12e-=2CO2↑+12H+,
故答案为:正;CH3OCH3+3H2O-12e-=2CO2↑+12H+.
点评 本题考查了化学平衡状态的判断、盖斯定律的应用、水解反应、电化学原理等,属于拼合型题目,侧重于考查学生对基础知识的综合应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 附着在试管内壁上的AgCl固体可用氨水溶解而洗去 | |
| B. | 可用氨水鉴别AlCl3、AgNO3和CuSO4三种溶液 | |
| C. | 向氨水中滴加CuSO4溶液至过量,先产生蓝色沉淀,然后沉淀溶解并得到深蓝色溶液 | |
| D. | 加热碘单质,产生紫色蒸气,这个过程克服了范德华力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解CuSO4溶液一段时间后,加入适量Cu(OH)2可以使溶液恢复至原状态 | |
| B. | 将钢闸门与直流电源的负极相连,可以防止钢闸门腐蚀 | |
| C. | 电解AlCl3、FeCl3、CuCl2的混合溶液,在阴极上依次析出Cu、Fe、Al | |
| D. | 铅蓄电池在充电时,连接电源正极的电极上发生:PbSO4+2e-═Pb+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
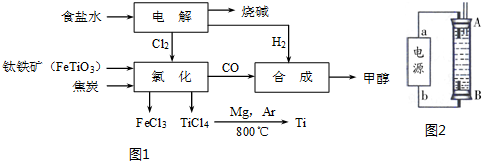
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制氢气,为了加快反应速率,可向稀 H2SO4 中滴加少量 Cu(NO3)2 溶液 | |
| B. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,平衡时氢气转化率增大 | |
| C. | 吸热反应“TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0 | |
| D. | 在稀AgNO3溶液中加入过量 NaCl溶液,产生白色沉淀,再加入少量 Na2S溶液,出现黑色沉淀,则加入Na2S溶液后 c(Ag+) 更小了 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+ | B. | K+ | C. | Cl- | D. | Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烷燃烧的热化学方程式可表示为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H=-2221.5 kJ•mol-1 | |
| B. | 正丁烷燃烧的热化学方程式可表示为:2C4H10(g)+18O2(g)=8CO2(g)+10H2O(l);△H=-2878 kJ•mol-1 | |
| C. | 正丁烷转化为异丁烷的过程是一个放热过程 | |
| D. | 正丁烷比异丁烷稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
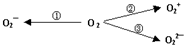

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com