
��14�֣���ʵ������������250mL0.1mol/L��Na2CO3��Һ,��ղ���ش��������⣺
��1������250mL0.1mol/L��Na2CO3��Һ
| ʵ��Ӧ��Na2CO3����/g | Ӧѡ������ƿ�Ĺ��/mL | ������ƿ���Ҫ���������� |
|
|
|
|
��2������ʱ������ȷ�IJ���˳���ǣ���ĸ��ʾ��ÿ����ĸֻ����һ�Σ� ___ _____��
A����30mLˮϴ���ձ�2��3�Σ�ϴ��Һ��ע������ƿ����
B����������ƽȷ��ȡ�����̼���Ƶ���������ˮ��Լ30mL���ܽ�
C�����ܽ�Һע������ƿ��
D��������ƿ�ǽ�����ҡ��
E����μ�ˮ��ʹ��Һ����ǡ����̶�����
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1��2cm��
��3������A�У���ϴ��Һ����������ƿ����Ŀ���� ��
��4�������������������������ҺŨ�Ƚ��к�Ӱ�죨�ƫ�ߡ�����ƫ�͡�����Ӱ�족��?��û�н���A���� ����������ˮʱ���������˿̶� ��������ʱ���ӿ̶���___________________������ʱ���������λ�÷Ŵ� ��Na2CO3 ���������ᾧˮ ��
��5����ʵ������г������������δ�����������ˮʱ���������˿̶� ��������ƿ��ת����Һʱ(ʵ�鲽���)������Һ�ε�������ƿ���� ��
 ѧ���쳵�����ּ��������ҵ�½����������ϵ�д�
ѧ���쳵�����ּ��������ҵ�½����������ϵ�д� �����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д� Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
Сѧ�����ҵ���ϴ�ѧ������ϵ�д� ���Ž�����ٰθ��νӹ㶫���������ϵ�д�
���Ž�����ٰθ��νӹ㶫���������ϵ�д� �����������ҵ�������������ϵ�д�
�����������ҵ�������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| m |
| 233 |
| V |
| 200 |
| m |
| 233 |
| V |
| 200 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
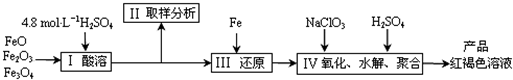
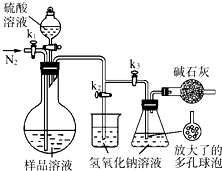 ��2013?������ģ��̼����-��������Ӻ��aNa2CO3?bH2O2������Ư�ס�ɱ�����ã�ʵ�����á����������Ʊ������ʵ�ʵ�鲽�����£�
��2013?������ģ��̼����-��������Ӻ��aNa2CO3?bH2O2������Ư�ס�ɱ�����ã�ʵ�����á����������Ʊ������ʵ�ʵ�鲽�����£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ���� | 0�� | 10�� | 20�� | 30�� | 40�� | 50�� | 60�� |
| FeSO4?7H2O | 15.6 | 20.5 | 26.5 | 32.9 | 40.2 | 48.6 | - |
| ��NH4��2SO4 | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | - | 88.0 |
| ��NH4��2SO4?FeSO4?6H2O | 12.5 | 17.2 | 21.0 | 28.1 | 33.0 | 40.0 | 44.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
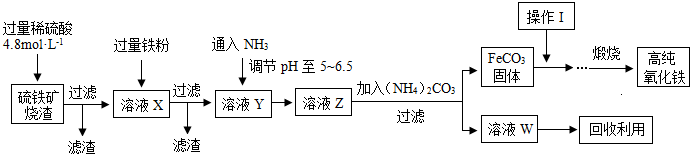
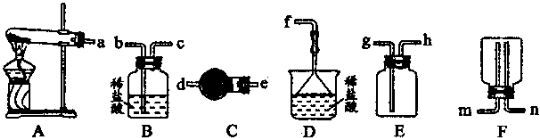
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�鲽�� | Ԥ������ͽ��� |
| ����1��ȡ����������A��B��֧�ྻ�Թ��У����� | ���������� |
| ����2����A�Թ��м��������Ba��OH��2��Һ�����ã����� | �а�ɫ���� |
| ����3��ȡ��������2�õ������������������ | ����������ȫ�ܽ⣬˵�������к������� |
| ����4��ȡ��������2�õ�����Һ�� |
|
| ����5����B�Թ��м��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com