
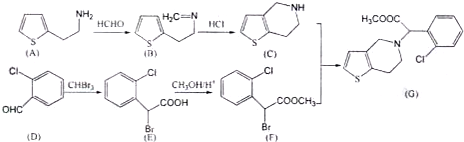
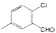
 )是D的一种同系物,在H的同分异构体中,同时满足下列条件的物质的结构简式为
)是D的一种同系物,在H的同分异构体中,同时满足下列条件的物质的结构简式为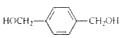 为起始原料,其他试剂任选,设计制备化合物
为起始原料,其他试剂任选,设计制备化合物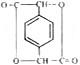 的合成路线图.
的合成路线图. )的同分异构体满足:②可与FeCl3溶液发生显色反应,含有酚羟基,①分子中只含1个环,则还含有碳碳双键,且有4中不同环境的H,故氯原子不可能连接苯环,故只能有2个取代基,除酚羟基外,另外的取代基只能有1种H原子,故为-CCl=CH2,且与酚羟基处于对位;
)的同分异构体满足:②可与FeCl3溶液发生显色反应,含有酚羟基,①分子中只含1个环,则还含有碳碳双键,且有4中不同环境的H,故氯原子不可能连接苯环,故只能有2个取代基,除酚羟基外,另外的取代基只能有1种H原子,故为-CCl=CH2,且与酚羟基处于对位; 应先制备
应先制备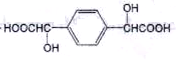 ,结合转化关系中D→E的转化可知,
,结合转化关系中D→E的转化可知, 发生氧化反应生成
发生氧化反应生成 ,再与CHBr3反应得到
,再与CHBr3反应得到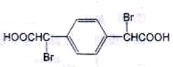 ,碱性条件下水解得到
,碱性条件下水解得到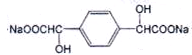 ,酸化得到
,酸化得到 ,再发生分子内酯化反应得到目标物质.
,再发生分子内酯化反应得到目标物质. ,
, ;
; )的同分异构体满足:②可与FeCl3溶液发生显色反应,含有酚羟基,①分子中只含1个环,则还含有碳碳双键,且有4中不同环境的H,故氯原子不可能连接苯环,故只能有2个取代基,除酚羟基外,另外的取代基只能有1种H原子,故为-CCl=CH2,且与酚羟基处于对位,该同分异构体的结构简式为:
)的同分异构体满足:②可与FeCl3溶液发生显色反应,含有酚羟基,①分子中只含1个环,则还含有碳碳双键,且有4中不同环境的H,故氯原子不可能连接苯环,故只能有2个取代基,除酚羟基外,另外的取代基只能有1种H原子,故为-CCl=CH2,且与酚羟基处于对位,该同分异构体的结构简式为: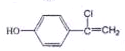 ,故答案为:
,故答案为: ;
; 应先制备
应先制备 ,结合转化关系中D→E的转化可知,
,结合转化关系中D→E的转化可知, 发生氧化反应生成
发生氧化反应生成 ,再与CHBr3反应得到
,再与CHBr3反应得到 ,碱性条件下水解得到
,碱性条件下水解得到 ,酸化得到
,酸化得到 ,再发生分子内酯化反应得到目标物质,合成路线流程图为:
,再发生分子内酯化反应得到目标物质,合成路线流程图为: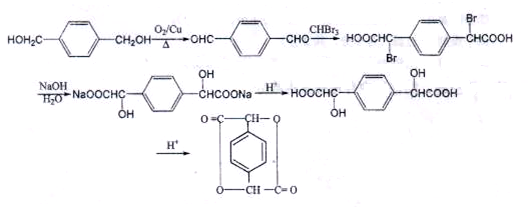 ,
, .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、500mL溶液中含SO42-、Fe3+总数为NA |
| B、500mL溶液中含0.6NA个SO42- |
| C、1L溶液中含有0.2NA个Fe3+ |
| D、500mL该溶液中SO42-物质的量浓度为0.6mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④⑥⑧ |
| B、①②⑤⑥⑦ |
| C、②③④⑥⑧ |
| D、③④⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、分子式为C8H10的芳香烃有3个,分别为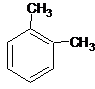 、 、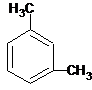 和 和 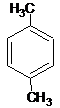 |
| B、分子式为C2H6O的同分异构体有两个,分别是 H3C-O-CH3 和 CH3CH2OH |
| C、分子式为C4H8的烯烃同分异构体有2个,分别为CH2=CHCH2CH3、CH3CH=CHCH3 |
D、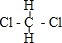 和 和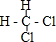 是两种不同的物质 是两种不同的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 共价键 | H-H | C-H | C≡C |
| 能量变化/kJ?mol-1 | 436 | 413 | 812 |
查看答案和解析>>
科目:高中化学 来源: 题型:
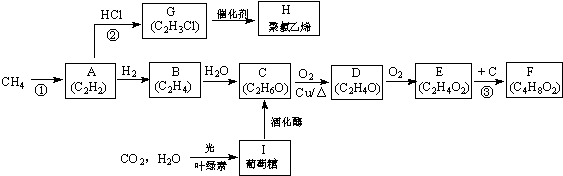
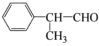 ,工业合成路线如下:
,工业合成路线如下: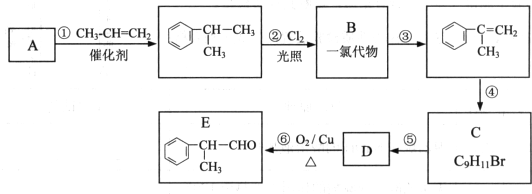
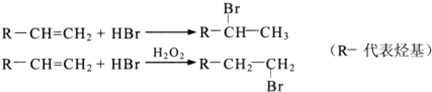
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
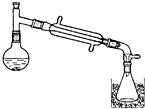 一溴乙烷为无色液体,熔点-119.1℃,沸点38.4℃,常用于汽油的乙基化、冷冻剂和麻醉剂.制备一溴乙烷的反应原理为:NaBr+H2SO4═HBr↑+NaHSO4,CH3CH2OH+HBr→CH3CH2Br+H2O.实验室可用如图装置制备一溴乙烷
一溴乙烷为无色液体,熔点-119.1℃,沸点38.4℃,常用于汽油的乙基化、冷冻剂和麻醉剂.制备一溴乙烷的反应原理为:NaBr+H2SO4═HBr↑+NaHSO4,CH3CH2OH+HBr→CH3CH2Br+H2O.实验室可用如图装置制备一溴乙烷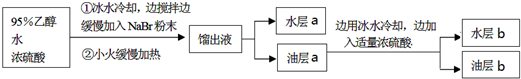
| 实验步骤 | 预期现象和结论 |
| 步骤1:将油层b转移至 | |
| 步骤2:取步骤1的水层少量于试管中,加入稀硫酸酸化,再加入适量新制氯水及少量CCl4,充分振荡,静置. | 溶液分层,下层呈橙红色,证明 |
| 步骤3:将步骤1的油层充分洗涤、干燥后装入蒸馏装置中, | 馏出蒸汽的温度稳定在38℃左右,不再有蒸汽馏出时,将蒸馏烧瓶中残留液体置于冰水浴中冷却,凝结成白色固体,则证明油层b中含有1,2-二溴乙烷. |
查看答案和解析>>
科目:高中化学 来源: 题型:
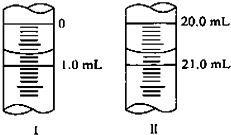 在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO- 4 |
2- 4 |
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com