

分析 (1)①pH=13时,c(S2-)=5.7×10-2mol/L,在0.10mol•L-1H2S溶液中根据硫守恒c(H2S)+c(HS-)+c(S2-)=0.10mol•L-1;
②当Qc=Ksp(MnS)时开始沉淀,由此求出硫离子的浓度,结合图象得出此时的pH;根据MnS和FeS的Ksp计算;
(2)①图象分析反应焓变是2mol二氧化硫完全反应法的热量.E为活化能,活化能的大小与反应热无关;加入催化剂能降低反应的活化能;
②计算此时反应的浓度商Q,和平衡常数比较判断反应进行的方向.
解答 解:(1)①根据溶液pH与c(S2-)关系图pH=13时,c(S2-)=5.7×10-2mol/L,在0.10mol•L-1H2S溶液中根据硫守恒c(H2S)+c(HS-)+c(S2-)=0.10mol•L-1,所以c(H2S)+c(HS-)=0.1-5.7×10-2=0.043mol/L,
故答案为:0.043;
②当Qc=Ksp(FeS)时开始沉淀,所以c(S2-)=$\frac{Ksp(FeS)}{c(Fe{\;}^{2+})}$=$\frac{1.4×10{\;}^{-19}}{0.01}$mol/L=1.4×10-17mol/L,结合图象得出此时的pH=2,所以pH=2时亚铁离子开始沉淀;
溶液中$\frac{c(M{n}^{2+})}{c(F{e}^{2+})}$=$\frac{Ksp(MnS)}{Ksp(FeS)}$=$\frac{2.8×10{\;}^{-13}}{1.4×10{\;}^{-19}}$mol/L=2×106;
故答案为:2;2×106;
(2)SO2(g)+$\frac{1}{2}$O2(g)═SO3(g)△H=-99kJ/mol,
①图Ⅱ分析可知2molSO2和氧气全部反应,反应焓变△H=-99kJ/mol×2mol=-198KJ,E为活化能,反应热可表示为A、C活化能的大小之差,活化能的大小与反应热无关;加入催化剂改变了反应的途径,降低反应所需的活化能,所以E的变化是减小;
故答案为:-198;因为催化剂改变了反应的历程使活化能E降低;
②该温度下,向100L的恒容密闭容器中,充入3.0mol SO2(g)、16.0mol O2(g)和3.0mol SO3(g),浓度商Qc=$\frac{\frac{3.0mol}{100L}}{\frac{3.0mol}{100L}×(\frac{16.0mol}{100L}){\;}^{\frac{1}{2}}}$=2.5<K=3.33,
则反应开始时(正)>v(逆)
故答案为:>.
点评 本题考查化学平衡常数及平衡状态的判断、燃料电池、氧化还原反应及滴定的相关知识,涉及的题量较大,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=14的溶液中:Na+、CO32-、Al3+、ClO- | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1010的溶液中:K+、Fe2+、Cl-、SO42- | |
| C. | 加入铝片能放出H2的溶液中:Na+、HCO3-、Cu2+、SO42- | |
| D. | 水电离出来的c(H+)=10-13mol•L-1的溶液中:NH4+、K+、NO3-、SiO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子体积的大小 | |
| B. | 分子间的间距变了分子间作用力的强弱变了 | |
| C. | 相对分子质量的大小 | |
| D. | 分子内共价键的长短 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 利用CO和H2在催化剂的作用下合成甲醇,反应如下:CO(g)+2H2(g)?CH3OH(g).在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示.下列说法正确的是( )
利用CO和H2在催化剂的作用下合成甲醇,反应如下:CO(g)+2H2(g)?CH3OH(g).在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示.下列说法正确的是( )| A. | 该反应的△H<0,且p1<p2<p3 | |
| B. | 在C点时,H2转化率为75% | |
| C. | 反应速率:ν逆(状态A)>ν逆(状态B) | |
| D. | 在恒温恒压条件下,向该密闭容器中再充入1molCH3OH,达平衡时CH3OH的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图Ⅰ表示t1时刻升高温度对反应速率的影响 | |
| B. | 图Ⅰ不能表示t1时刻增大C物质的浓度对反应速率的影响 | |
| C. | 图Ⅱ一定表示的是在t1时刻使用了催化剂对反应速率的影响 | |
| D. | 图Ⅲ表示温度对A的转化率的影响,且乙的温度比甲的温度高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,向20mL的某稀盐酸中滴入0.1mol•L-1的氨水,溶液中由水电离出的氢离子浓度随滴人氨水体积的变化如图.下列分析不正确的是( )
常温下,向20mL的某稀盐酸中滴入0.1mol•L-1的氨水,溶液中由水电离出的氢离子浓度随滴人氨水体积的变化如图.下列分析不正确的是( )| A. | V2=20 mL | B. | d点溶液中:c(NH4+)>c(Cl-) | ||
| C. | b点溶液中:c(H+)=c(OH-) | D. | 该稀盐酸的浓度为0.1 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,基态f原子的核外电子排布式为1s22s22p63s23p63d104s1.
,基态f原子的核外电子排布式为1s22s22p63s23p63d104s1.
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
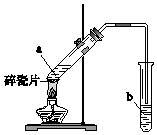 实验室用如图所示装置制备乙酸乙酯.
实验室用如图所示装置制备乙酸乙酯. 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com