
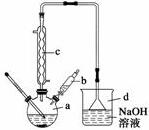
 溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:
溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:| 苯 | 溴 | 溴苯 | |
| 密度/gcm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中的溶解度 | 微溶 | 微溶 | 微溶 |
 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr.
+HBr.分析 (1)实验室合成溴苯是苯与液溴在铁粉作催化剂的条件下发生取代反应生成溴苯和溴化氢;
(2)根据该反应为放热反应及苯、溴的沸点较低容易挥发进行分析;
(3)根据表中数据可知,苯和液溴的沸点较低,容易变成气体挥发出来,仪器c的作用是冷凝回流,仪器d是吸收挥发出的HBr;
(4)分离出的粗溴苯中含有未反应的苯,分离互溶的液体,根据沸点不同,利用蒸馏的方法进行分离.
解答 解:(1)在a中加入15mL苯和少量铁屑,再将b中4.0mL液溴慢慢加入到a中,充分反应生成溴苯和溴化氢,反应的化学方程式为 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr,
+HBr,
故答案为: +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr;
+HBr;
(2)苯与液溴的反应为放热反应,若加入液溴速度过快,反应会放出较多的热量,由于苯和溴的沸点较低,导致苯和溴会挥发出来,影响了溴苯的产率,将b中的液溴慢慢加入到a中,防止反应放出的热使C6H6、Br2挥发而影响产率,
故答案为:C6H6、Br2;
(3)苯的沸点为80℃,溴的沸点为59℃,二者沸点较低,容易挥发出来,仪器c冷凝器的作用是冷凝回流C6H6、Br2,仪器d中发生的主要反应是吸收HBr气体,防污染防倒吸,
故答案为:冷凝回流;吸收HBr防污染防倒吸;
(4)利用沸点不同,苯的沸点小,被蒸馏出,溴苯留在母液中,所以采取蒸馏的方法分离溴苯与苯,故答案为:蒸馏.
点评 本题考查了苯的性质、制备实验方案的设计,题目难度中等,涉及了溴苯的制取实验、物质的分离提纯等,清楚制备的原理是解答的关键,充分培养了学生的分析、理解能力及灵活应用所学知识解决问题的能力.


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:解答题
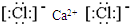 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | C | D | E | F | G | |
| A | - | - | - | - | - | - | ↓ |
| B | - | - | - | - | - | ↓ | ↓ |
| C | - | - | - | ↓ | - | ↓ | ↓ |
| D | - | - | ↓ | - | ↓ | ↓ | ↓ |
| E | - | - | - | ↓ | - | ↓ | - |
| F | - | ↓ | ↓ | ↓ | ↓ | - | ↓ |
| G | ↓ | ↓ | ↓ | ↓ | - | ↓ | - |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 样品中只含有一种杂质NaHCO3 | B. | 样品中含有KCl,不含有NaHCO3 | ||
| C. | 样品中含有Ba(NO3)2和NaHCO3 | D. | 样品中含有KCl和NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CH2=CH3 | B. | CH2=CH-CH2OH | C. | CH3=CH-COOH | D. | CH2=CH-COOCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
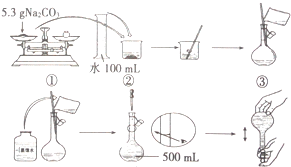 某兴趣小组为探究Na2CO3溶液的性质,需要480mL0.2mol•L-1的Na2CO3溶液.溶液的配制过程如图所示:
某兴趣小组为探究Na2CO3溶液的性质,需要480mL0.2mol•L-1的Na2CO3溶液.溶液的配制过程如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电子由铁棒通过导线流向铜棒 | B. | 正极反应为Fe-2e-═Fe2+ | ||
| C. | 铜棒逐渐溶解 | D. | 该装置能将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
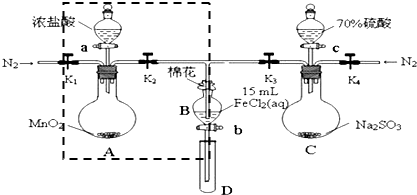
| 过程⑤B溶液中含有的离子 | 过程⑦B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com