
| A. | 为了增强高锰酸钾溶液的氧化能力,用稀盐酸将高锰酸钾溶液进行酸化 | |
| B. | 欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 | |
| C. | 用稀盐酸洗涤盛放过石灰水的试剂瓶 | |
| D. | 欲配制质量分数为10%的ZnSO4溶液,将10 g ZnSO4•7H2O溶解在90 g水中 |
分析 A.稀盐酸与高锰酸钾溶液发生氧化还原反应;
B.长时间煮沸发生胶体的聚沉;
C.盛放过石灰水的试剂瓶,内壁有碳酸钙;
D.将10gZnSO4•7H2O溶解在90g水中,溶液质量为100g,但溶质ZnSO4的质量小于10g.
解答 解:A.稀盐酸与高锰酸钾溶液发生氧化还原反应,则为了增强高锰酸钾溶液的氧化能力,用稀硫酸将高锰酸钾溶液进行酸化,故A错误;
B.长时间煮沸发生胶体的聚沉,则向盛有沸水的烧杯中滴加FeCl3饱和溶液出现红褐色液体即得到胶体,故B错误;
C.盛放过石灰水的试剂瓶,内壁有碳酸钙,与酸反应,则用稀盐酸洗涤盛放过石灰水的试剂瓶,故C正确;
D.将10gZnSO4•7H2O溶解在90g水中,溶液质量为100g,但溶质ZnSO4的质量小于10g,则质量分数小于10%,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及氧化还原反应、胶体制备、物质的性质、溶液配制等,把握物质的性质、反应原理及实验技能为解答的关键,侧重分析与实验能力的考查,选项A为易错点,题目难度不大.


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 砹是一种有色固体,它的气态氢化物很不稳定 | |
| B. | F2与水反应比Cl2与水反应剧烈 | |
| C. | 铷的最高价氧化物的水化物一定是强碱 | |
| D. | 由盐酸的酸性比氢硫酸强可推知氯的非金属性强于硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 相关微粒浓度关系:c(X-)=c(Y-)+c(HY)=c(Z-)+c(HZ) | |
| B. | 三种溶液所含阴阳离子的总数依次减小 | |
| C. | 三种溶液均加水稀释到1000mL,pH分别变为8、9、10 | |
| D. | HX、HY、HZ的酸性依次增强,电离平衡常数依次减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采用加热方法消毒的目的是使蛋白质变性而杀灭细菌 | |
| B. | 石油分馏可得到石油气、汽油、煤油、柴油等 | |
| C. | “海水淡化”可以解决“淡水供应危机”,加入明矾可以使海水淡化 | |
| D. | 已知Ksp(MnS)>Ksp(CdS) 所以工业上用MnO2制取MnCl2时,用MnS除去溶液中含有的Cd2+离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
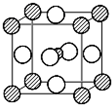
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
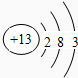 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
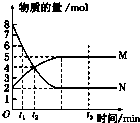 一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com