
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl﹣、Mg2+、
Ba2+、CO32﹣、SO42﹣ , 现取三份100mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生
②第二份加足量NaOH溶液加热后,收集到气体0.04mol
③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.
试回答下列问题
(1)由实验②可知溶液中含有的离子为 , 在100mL溶液中该离子的物质的量浓度为
(2)由实验③可以判断中溶液中含有的离子为
(3)由上述实验信息判断下列说法中正确的是。
A.K+一定存在
B.100mL溶液中含0.01mol CO32﹣
C.Cl﹣可能存在
D.Ba2+一定不存在,Mg2+可能存在.
(4)根据上述实验,该溶液中是否有不能肯定其存在的离子?若有,则为进一步确定其存在,应该补充的实验是 .
【答案】
(1)NH4+;0.4mol/L
(2)CO32﹣、SO42﹣
(3)A,C
(4)取少量原溶液,加入足量Ba(NO3)2溶液后,静置取上层清液加入AgNO3溶液和稀HNO3 , 如果有沉淀产生说明存在Cl﹣
【解析】解:①第一份加入AgNO3溶液有沉淀产生,与AgNO3溶液有沉淀产生的离子有:Cl﹣、CO32﹣、SO42﹣;②加足量NaOH溶液加热产生气体,气体是氨气,故一定有铵离子0.04mol,溶液中一定含有NH4+ , 并且物质的量为0.04mol;③不溶于盐酸的2.33g为硫酸钡,物质的量为: ![]() =0.01mol;6.27g沉淀是硫酸钡和碳酸钡,碳酸钡质量为6.27g﹣2.33g=3.94g,碳酸钡的物质的量为:
=0.01mol;6.27g沉淀是硫酸钡和碳酸钡,碳酸钡质量为6.27g﹣2.33g=3.94g,碳酸钡的物质的量为: ![]() =0.02mol,故原溶液中一定存在CO32﹣、SO42﹣ , 则一定没有Mg2+、Ba2+;再根据电荷守恒,正电荷为:n(+)=n(NH4+)=0.04mol;c(﹣)=2c(CO32﹣)+2c(SO42﹣)=0.06mol,正电荷总物质的量大于负电荷,故原溶液中一定有K+ , 至少为0.02mol;综合以上可以得出,一定存在的离子有:NH4+、K+、CO32﹣、SO42﹣ , 一定没有的离子Mg2+、Ba2+ , 可能存在Cl﹣ , (1)由实验②可知溶液中含有0.04molNH4+ , 在100mL溶液中该离子的物质的量浓度为:
=0.02mol,故原溶液中一定存在CO32﹣、SO42﹣ , 则一定没有Mg2+、Ba2+;再根据电荷守恒,正电荷为:n(+)=n(NH4+)=0.04mol;c(﹣)=2c(CO32﹣)+2c(SO42﹣)=0.06mol,正电荷总物质的量大于负电荷,故原溶液中一定有K+ , 至少为0.02mol;综合以上可以得出,一定存在的离子有:NH4+、K+、CO32﹣、SO42﹣ , 一定没有的离子Mg2+、Ba2+ , 可能存在Cl﹣ , (1)由实验②可知溶液中含有0.04molNH4+ , 在100mL溶液中该离子的物质的量浓度为: ![]() =0.4mol/L,所以答案是:NH4+;0.4mol/L;(2)由实验③可以判断中溶液中一定存在CO32﹣、SO42﹣ , 则一定没有Mg2+、Ba2+ , 所以答案是:CO32﹣、SO42﹣;(3)A.根据分析可知,溶液中一定存在K+ , 故A正确; B.100mL溶液中含0.02mol CO32﹣ , 故B错误; C.溶液中可能含有Cl﹣ , 故C正确; D.溶液中一定没有Mg2+、Ba2+ , 故D错误;所以答案是:AC;(4)溶液中可能含有氯离子,检验原溶液中是否含有氯离子的操作方法为:取少量原溶液,加入足量Ba(NO3)2溶液后,静置取上层清液加入AgNO3溶液和稀HNO3 , 如果有沉淀产生说明存在Cl﹣ , 所以答案是:取少量原溶液,加入足量Ba(NO3)2溶液后,静置取上层清液加入AgNO3溶液和稀HNO3 , 如果有沉淀产生说明存在Cl﹣ .
=0.4mol/L,所以答案是:NH4+;0.4mol/L;(2)由实验③可以判断中溶液中一定存在CO32﹣、SO42﹣ , 则一定没有Mg2+、Ba2+ , 所以答案是:CO32﹣、SO42﹣;(3)A.根据分析可知,溶液中一定存在K+ , 故A正确; B.100mL溶液中含0.02mol CO32﹣ , 故B错误; C.溶液中可能含有Cl﹣ , 故C正确; D.溶液中一定没有Mg2+、Ba2+ , 故D错误;所以答案是:AC;(4)溶液中可能含有氯离子,检验原溶液中是否含有氯离子的操作方法为:取少量原溶液,加入足量Ba(NO3)2溶液后,静置取上层清液加入AgNO3溶液和稀HNO3 , 如果有沉淀产生说明存在Cl﹣ , 所以答案是:取少量原溶液,加入足量Ba(NO3)2溶液后,静置取上层清液加入AgNO3溶液和稀HNO3 , 如果有沉淀产生说明存在Cl﹣ .


 一课一练课时达标系列答案
一课一练课时达标系列答案 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。

图1 图2
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择_____________________(填字母)。
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:_________________________。
(2)图2中,钢闸门C作_____________极。若用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应为____________________,检测该电极反应产物的方法是___________________________。

图3 图4
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的______极(填“正”或“负”)。F电极上的电极反应为_____________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室要配制2mol/L稀硫酸250mL.
(1)需要量取质量分数为98%密度为1.84g/mL的浓硫酸mL.
(2)配制过程中除了烧杯量筒,玻璃棒,还需要哪些仪器
(3)容量瓶使用前应先检漏,请简述捡漏的操作方法
(4)下列实验操作中,按先后顺序排列为 . A.将稀释、冷却后的硫酸沿玻璃棒注入250mL容量瓶中.
B.将洗涤液也注入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀.
C.将量取的浓硫酸沿玻璃棒缓慢注入烧杯中,搅拌并冷却至室温.
D.向烧杯中加入约100mL蒸馏水.
E.用适量蒸馏水洗涤烧杯2~3次.
F.向容量瓶中加蒸馏水到液面接近刻度1cm~2cm处.
G.盖上瓶塞,并反复倒转摇匀.
H.用胶头滴管加蒸馏水到瓶颈刻度处.
(5)由于错误操作,判断得到的实际浓度与理论数据的偏差(填偏大,偏小或无影响) A、用量筒量取一定量液体时,俯视液面读数
B、容量瓶刚用蒸馏水洗净,没有烘干
(6)最后将所配溶液存放在试剂瓶中,并贴上标签,请你填写该标签(如图). 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。下图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是( )
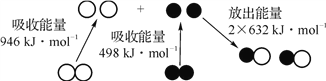
A. 放电条件下,N2(g)和O2(g)混合能直接化合生成NO(g)
B. NO是一种酸性氧化物,能用NaOH溶液处理含NO的尾气
C. N2(g)和O2(g)反应生成 NO(g),相当于N2(g)在O2(g)燃烧,该反应放热
D. 28 g N2(g)和32 g O2(g)完全反应生成 NO(g),放出的能量为180 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,0. molNa2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示。下列有关溶液中离子浓度关系叙述正确的是( )

A. W点所示的溶液中:c(CO32-)=c(HCO3-)>c(OH-)>c(H+)
B. pH=14的溶液中:c(H2CO3)+c(HCO3-)+c(CO32-)=0.1mol/L
C. pH=8的溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-)
D. pH=11的溶液中:c(Na+)+ c(H+)=c(OH-)+c(Cl-)+c(CO32-)+c(HCO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用锌粒和稀硫酸反应制取氢气,下列措施不能使反应速率加快的是( )
A.降低反应温度
B.滴加少量硫酸铜溶液
C.适当的增加硫酸的浓度
D.锌粉代替锌粒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中,发生可逆反应mA(g)+nB(g)![]() pC(g)+qD(s),当
pC(g)+qD(s),当
m、n、p、q为任意整数时,反应达到平衡的标志是( )
①体系的压强不再改变 ②体系的温度不再改变 ③体系的密度不再变化 ④各组分质量分数不再改变
A. ①②③ B. ①②④ C. ②③④ D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】许多古代文学中都蕴含着科学知识,下列对古文学的解释不正确的是( )
A. 李时珍在《本草纲目》中对火药的描述是:“味辛、酸,有小毒。主疮癣,杀虫,辟湿气温疫。乃焰消、硫黄、杉木炭所合,以为烽燧铳机诸药者。”该描述中的“焰消”指的是硝酸钾。
B. 沈括《梦溪笔谈》:“凡铁之有钢者,如面中有筋,濯尽柔面,则面筋乃见,炼钢亦然。但取精铁锻之百余火,每锻称之,一锻一轻,至累锻而斤两不减,则纯钢也,虽百炼,不耗矣。”该描述中的“一锻一轻”是由于铁中含碳量降低。
C. 晋代葛洪的《抱朴子》记载“丹砂烧之成水银,积变又成丹砂”,是指加热时丹砂(HgS)熔融成液态,冷却时重新结晶为HgS晶体。
D. 北宋诗人苏轼在《石炭并引》记载:“投泥泼水愈光明,烁玉流金见精悍。南山栗林渐可息,北山顽矿何劳锻。为君铸作百炼刀,要斩长鲸为万段。”该描述中“投泥泼水愈光明”是指高温时碳与水蒸气反应生成氢气和一氧化碳,两种可燃性气体燃烧。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com