
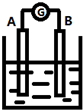
 ��ͼΪԭ���װ��ʾ��ͼ��
��ͼΪԭ���װ��ʾ��ͼ������ ��1����ԭ����У�пʧ���ӱ�����ӽ�����Һ������п����A��Ϊ������ʯīΪ�����������������ӵõ�������������
��2����ԭ����У���Ƭʧ���ӱ�ɶ��������ӽ�����Һ��������Ƭ��������ͭƬ�����������������������ӵõ������ɶ��������ӣ�
��3����ԭ�����ʧ���ӵ�һ��Ϊ�������õ��ӵ�һ��Ϊ������������ȼ�ϵ���У������õ��ӣ�����ͨ��������һ��Ϊ�õ�ص�������������������Ӧ����ˮ���缫��Ӧʽ��ӵõ�ط�Ӧʽ��
��4�����ݵ�ط�Ӧʽ֪��PbԪ�ػ��ϼ���0�ۡ�+4�۱�Ϊ+2�ۣ��õ��ӻ��ϼ۽��͵ķ�Ӧ��Ϊ������ʧ���ӻ��ϼ����ߵĽ���Ϊ������������PbO2�õ��Ӻ�H2SO4��Ӧ����PbSO4����·��ת��2mol e-�����ݷ���ʽ��������H2SO4�����ʵ�����
��� �⣺��1����ԭ����У�пʧ���ӱ�����ӽ�����Һ������п����A��Ϊ������ʯīΪ�����������������ӵõ����������������Ե缫��ӦʽΪ2H++2e-=H2�����ʴ�Ϊ��������2H++2e-=H2����
��2����ԭ����У���Ƭʧ���ӱ�ɶ��������ӽ�����Һ���缫��ӦʽΪ Fe-2e-=Fe2+��������Ƭ��������ͭƬ�����������������������ӵõ������ɶ��������ӣ��缫��ӦʽΪ2Fe3++2 e-=2Fe2+���ʴ�Ϊ������2Fe3++2 e-=2Fe2+��Fe-2e-=Fe2+��
��3����ԭ�����ʧ���ӵ�һ��Ϊ�������õ��ӵ�һ��Ϊ������������ȼ�ϵ���У������õ��ӣ�����ͨ��������һ��Ϊ�õ�ص�������������������Ӧ����ˮ�����Ե�ط�ӦʽΪ2H2+O2=2H2O���ʴ�Ϊ������2H2+O2=2H2O��
��4�����ݵ�ط�Ӧʽ֪��PbԪ�ػ��ϼ���0�ۡ�+4�۱�Ϊ+2�ۣ�ʧ���ӻ��ϼ����ߵĽ���Ϊ��������PbΪ�������ŵ�ʱ��������PbO2�õ��Ӻ�H2SO4��Ӧ����PbSO4���缫��ӦʽΪPbO2+2e-+4H++SO42-=PbSO4+2H2O����·��ת��2mole-������4mol�����ӣ���2mol���ᣬ�ʴ�Ϊ��Pb��PbO2+2e-+4H++SO42-=PbSO4+2H2O��2��
���� ���⿼����ԭ��ص����������жϼ��缫��Ӧʽ����д�������֪ʶ�㣬д�缫��ӦʽʱҪע��������Һ�ijɷ֣�


 ���100�ֵ�Ԫ�Ż�������ϵ�д�
���100�ֵ�Ԫ�Ż�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
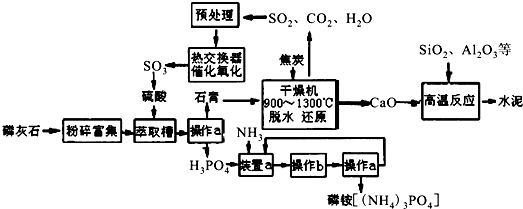
 | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
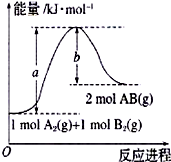 ��1����֪��ѧ��ӦA2��g��+B2��g��=2AB��g���������仯��ͼ��ʾ���÷�Ӧ���Ȼ�ѧ����ʽΪA2��g��+B2��g��=2AB��g����H=��a-b��kJ/mol��
��1����֪��ѧ��ӦA2��g��+B2��g��=2AB��g���������仯��ͼ��ʾ���÷�Ӧ���Ȼ�ѧ����ʽΪA2��g��+B2��g��=2AB��g����H=��a-b��kJ/mol���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
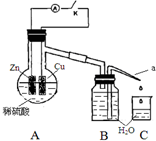 ��ͬѧ������װ�ý���ʵ�飬����Ӱ�췴Ӧ���ʵ����أ�
��ͬѧ������װ�ý���ʵ�飬����Ӱ�췴Ӧ���ʵ����أ�| ʵ��Ͽ�K��1����ˮ���� | 34 | 59 | 86 | 117 | �� | 102 |
| ʵ��պ�K��1����ˮ���� | 58 | 81 | 112 | 139 | �� | 78 |
| A�� | ʵ����л�ѧ����Ҫת��Ϊ���� | |
| B�� | ʵ����л�ѧ����Ҫת��Ϊ���� | |
| C�� | ��Ӧǰ��ˮ����58��34��81��59����Ҫԭ����ʵ������γ�ԭ��ؼӿ췴Ӧ���� | |
| D�� | ��Ӧ����ˮ����102��78����Ҫԭ����ʵ�����Һ�¶ȸ���ʵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬ����Ԫ�ص�ԭ�Ӱ뾶�� VIIA ���Ϊ��� | |
| B�� | �����ڱ�������Ԫ�صĵ���ȫ�������� | |
| C�� | IA��IIA ��Ԫ�ص�ԭ�ӣ���뾶Խ���Խ���õ��� | |
| D�� | ��������Ԫ�ص��������������������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʹ�ú��ʵĴ������ԼӴ�Ӧ���� | |
| B�� | ͨ�������O2����ʹSO2ת���ʴﵽ100% | |
| C�� | �����¶ȿ�������Ӧ���� | |
| D�� | ����O2Ũ�ȿ�������Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������������Ʒֱ���ȫȼ�գ����߷ų��������� | |
| B�� | ������ȼ����Ϊ285.5 kJ/mol��������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g���T2H2O��l����H=-285.8 kJ/mol | |
| C�� | Ba��OH��2•8H2O��s��+2NH4Cl��s���T=BaCl2��s��+2NH3��g��+10H2O��l����H��0 | |
| D�� | ��֪�к���Ϊ57.3 kJ/mol��������0.5 mol H2SO4��Ũ��Һ�뺬1 mol NaOH����Һ��ϣ��ų�������Ҫ����57.3 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
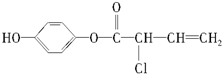 ���й�M��������������ȷ���ǣ�������
���й�M��������������ȷ���ǣ�������| A�� | ����H2��Ӧ��1 mol M�������5 mol H2 | |
| B�� | ����Ũ��ˮ��Ӧ��1 mol M�������4 mol Br2 | |
| C�� | ����NaOH��Һ��Ӧ��1 mol M�������4 mol NaOH | |
| D�� | M����ʹ���Ը��������Һ��ɫ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com