
| A�� | ���������ݻ����䣬�������ټ���1mol H2����Ӧ���ʼӿ죬����������Ӧ��������Ũ�ȣ���Ӧ���ʼӿ� | |
| B�� | ��������������ѹǿ���䣬�����м���1mol N2��N2���μӷ�Ӧ������Ӧ���ʼ����������DZ���ѹǿ���䣬�����г���N2��������Ӧ��Ũ�ȼ�С����Ӧ���ʼ��� | |
| C�� | ���������ݻ����䣬�����м���1mol N2��N2���μӷ�Ӧ������Ӧ���ʲ��䣬�����Ƿ�Ӧ���Ũ�Ȳ��䣬��Ӧ���ʲ��� | |
| D�� | ��������������ѹǿ���䣬�������ټ���1mol H2��g����1mol I2��g������Ӧ���ʼ�С������������������Ӧ��Ũ�ȱ�С����Ӧ���ʼ�С |
���� �ں㶨�¶��£���Ӧ���ʵ�Ӱ������ȡ����Ũ�Ⱥ�ѹǿ��Ũ��Խ��Ӧ����Խ����ͨ��������壬�μӷ�Ӧ�����ʵ�Ũ�Ȳ��䣬��Ӧ���ʲ��䣬��ѹǿ���䣬ͨ��������壬���������Ӧ���Ũ�ȼ�С����Ӧ���ʼ�С���Դ˽����⣮
��� �⣻A�����������ݻ����䣬�����м���1molH2����Ӧ��Ũ������Ӧ��������A��ȷ��
B����������������ѹǿ���䣬�����м���1molN2���������Ӧ���Ũ�ȼ�С����Ӧ���ʼ�С����B��ȷ��
C�����������ݻ����䣬�����м���1molN2���μӷ�Ӧ�����ʵ�Ũ�Ȳ��䣬��Ӧ���ʲ��䣬��C��ȷ��
D����������������ѹǿ���䣬�����м���1 mol H2��g����1molI2��g�������������Ϊ2�������ʵ�������Ϊ2������Ũ�Ȳ��䣬��Ӧ���ʲ��䣬��D����
��ѡD��
���� ���⿼�黯ѧ��Ӧ���ʣ�Ϊ��Ƶ���㣬������Ӱ�����صĿ��飬�Ѷ��еȣ�ע�����Ӱ�����أ��״���ΪB��C��ע�����������ص㣮


 �ο�������ϵ�д�
�ο�������ϵ�д� ������ѧ��ʱ��ҵϵ�д�
������ѧ��ʱ��ҵϵ�д� ���������ʱ��ѵϵ�д�
���������ʱ��ѵϵ�д� �㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
�㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1�� | B�� | 2�� | C�� | 3�� | D�� | 5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ�仯һ�����������仯 | |
| B�� | ��ѧ�仯һ���л�ѧ���Ķ��Ѻ����� | |
| C�� | ��ѧ�仯һ���������ʵ�״̬�仯 | |
| D�� | ��ѧ�仯һ�������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
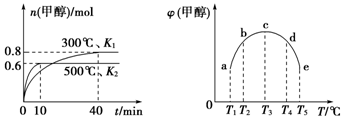
| A�� | �÷�Ӧ�ġ�H1��0����K1��K2 | |
| B�� | ������c�е�ƽ��״̬ת�䵽����d�е�ƽ��״̬���ɲ�ȡ�Ĵ�ʩ�����»��ѹ | |
| C�� | 300��ʱ����ƽ�����������ٳ���0.8 mol CO��0.6 mol H2��0.2 mol CH3OH��ƽ�������ƶ� | |
| D�� | 500��ʱ����ƽ�����������ٳ���1 mol CH3OH������ƽ���H2Ũ�ȺͰٷֺ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.5mol/L | B�� | 0.01mol/L | C�� | 0.02mol/L | D�� | 0.05mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��� | B�� | ��Ƿ� | C�� | ̿�� | D�� | ��ľ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �������� | NO3- | SO42- | H+ | M |
| Ũ��/��mol•L-1�� | 2 | 1 | 2 | 1 |
| A�� | Mg2+ | B�� | Ba2+ | C�� | H+ | D�� | S2- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com