

| ������ | Fe3+ | Fe2+ | Zn2+ | Cu2+ |
| ��ʼ����ʱ��pH | 2.7 | 6.6 | 5.2 | 4.4 |
| ������ȫʱ��pH | 3.7 | 8.9 | 8.1 | 5.7 |
���� ��ʵ�����̿�֪��п��ʯ�ڿ����б��գ�����������SO2����������Ʊ����ᣬ��п��ɰ����Ҫ��ZnO��ZnFe2O4����������FeO��CuO������������������ӦZnO+H2SO4=ZnSO4+H2O��FeO+H2SO4=FeSO4+H2O��CuO+H2SO4=CuSO4+H2O��ZnFe2O4+8H+=Zn2++2Fe3++4H2O������Һ�м����Լ�AΪ˫��ˮ��������Ӧ2Fe2++2H++H2O2=2 Fe3++2H2O��������Һ��pH��Fe3+ת��ΪFe��OH��3������������ҺpHʱ���������µ����ʣ����Լ�BΪZnO��ZnCO3��Zn��OH��2��Ȼ������Һ�м����Լ�CΪZn�������û���ͭ��Ȼ����ˣ������õ�Zn���Դ˽����⣮
��� �⣺��1��Ϊ�˼ӿ�п��ʯ���յ����ʣ��ɲ�ȡ�Ĵ�ʩ�н�п��ʯ�����ϸ�����������¶ȡ�����������ٵȣ�
�ʴ�Ϊ����п��ʯ�����ϸ������
��2���Լ�A��-��������Ԫ����ɵ�Һ̬����ɫ����������������Լ�A������Ӧ�����ӷ���ʽΪ2Fe2++2H++H2O2=2 Fe3++2H2O���Լ�B���ѡ��ZnO��ZnCO3��Zn��OH��2���ɱ������ݿ�֪��pH�ĵ��ط�ΧΪ3.7��pH��4.4��
�ʴ�Ϊ��2Fe2++2H++H2O2=2 Fe3++2H2O��ZnO��ZnCO3��Zn��OH��2��3.7��pH��4.4��
��3��������������֪������Zn�������û���ͭ����Ӧ�����ӷ���ʽΪCu2++Zn=Cu+Zn2+���Լ�C��Zn������������������ʧȥ���ӣ�������п���ӵõ����ӣ��������п��Һʱ����������һ�����ʿ�ѭ��ʹ�ã���������H2SO4��
�ʴ�Ϊ��Zn��H2SO4��
��4�����ʱ��ZnFe2O4�����������Σ��÷�Ӧ�Ļ�ѧ����ʽΪZnFe2O4+4H2SO4�TZnSO4+Fe2��SO4��3+4H2O���ʴ�Ϊ��ZnFe2O4+4H2SO4�TZnSO4+Fe2��SO4��3+4H2O��
��5���������ɵ�Fe��OH��3���壨���������������ԣ������ɵij����л�������Һ�е��������ʣ�
�ʴ�Ϊ��Fe��OH��3���壨���������������ԣ�
��6����0.1tп��ɰͨ���������̴��������յõ���21.4kg������ΪFe��OH��3����ԭ���غ��֪n��Fe��=$\frac{21.4��1000g}{107g/mol}$=200mol��������ȫת������п��ɰ����Ԫ�ص������������Ϊ$\frac{200mol��56g/mol}{0.1��1{0}^{6}g}$��100%=11.2%��
�ʴ�Ϊ��11.2%��
���� �����ۺϿ������ʵ��Ʊ��Լ����������ᴿ��Ϊ�߿��������ͣ���Ŀ������ȡ����п�����̿��������ӷ���ʽ����ѧ����ʽ����д��֪ʶ��ע���������������Ϣ����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH����ʼ������ | 1.9 | 7.15 | -0.23 | 3.4 |
| pH����ȫ������ | 3.2 | 9.15 | 1.09 | 4.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
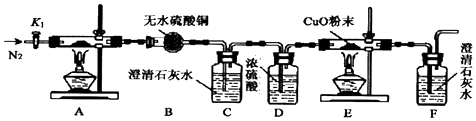
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
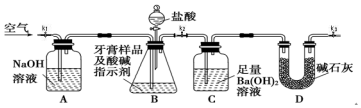
| ʵ�鲽�� | Ԥ����������� |
| ȡ����������Ʒ���Թ��У�����������NaOH��Һ�����ˣ�����Һ�еμ����ᣮ | ��Һ���ȳ��ְ�ɫ�������������ܽ⣬˵��������Ħ�����к����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
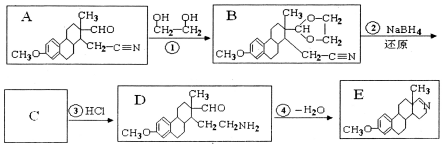
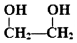 ������Ϊ�Ҷ�����д������Ա������ᷴӦ���ɸ߾���Ļ�ѧ����ʽ
������Ϊ�Ҷ�����д������Ա������ᷴӦ���ɸ߾���Ļ�ѧ����ʽ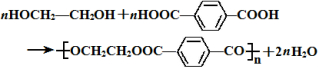 ��
��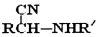 $\stackrel{H+}{��}$
$\stackrel{H+}{��}$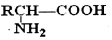
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com