
·ÖĪö ¢ŁŅĄ¾ŻøßĆĢĖį¼ŲČÜŅŗµÄŃÕÉ«Ą“ÖøŹ¾·“Ó¦ÖÕµć£¬µĪČė×īŗóŅ»µĪøßĆĢĖį¼ŲČÜŅŗ±ä»ÆĪŖ×ĻŗģÉ«£¬°ė·ÖÖÓ²»ĶŹÉ«ĖµĆ÷“ļµ½·“Ó¦ÖÕµć£»
¢ŚŅĄ¾ŻµĪ¶ØŹµŃéµÄ·“Ó¦ÖÕµćŹ±·¢ÉśµÄ·“Ó¦½ųŠŠ¼ĘĖć£¬ŅĄ¾ŻĢśŌŖĖŲŹŲŗć£¬½įŗĻµĪ¶Ø¹ż³ĢµÄ·“Ó¦Ąė×Ó·½³ĢŹ½¼ĘĖćµĆµ½£®
½ā“š ½ā£ŗ¢ŁŅĄ¾ŻøßĆĢĖį¼ŲČÜŅŗµÄŃÕÉ«Ą“ÖøŹ¾·“Ó¦ÖÕµć£¬µĪČė×īŗóŅ»µĪøßĆĢĖį¼ŲČÜŅŗ±ä»ÆĪŖ×ĻŗģÉ«£¬°ė·ÖÖÓ²»ĶŹÉ«ĖµĆ÷“ļµ½·“Ó¦ÖÕµć£¬
¹Ź“š°øĪŖ£ŗµ±µĪČė×īŗóŅ»µĪøßĆĢĖį¼ŲČÜŅŗ±ä»ÆĪŖ×ĻŗģÉ«£¬°ė·ÖÖÓ²»ĶŹÉ«ĖµĆ÷“ļµ½·“Ó¦ÖÕµć£»
¢Śa£®³ĘČ”5.7gĀĢ·Æ²śĘ·£¬Čܽā£¬ŌŚ250mLČŻĮæĘæÖŠ¶ØČŻ£»
b£®ĮæČ”25.00mL“ż²āČÜŅŗӌ׶ŠĪĘæÖŠ£»
c£®ÓĆĮņĖįĖį»ÆµÄ0.01000mol/L KMnO4ČÜŅŗµĪ¶ØÖĮÖÕµć£¬ĻūŗÄKMnO4ČÜŅŗĢå»żµÄĘ½¾łÖµĪŖ40.00mL£»
ŅĄ¾Ż·“Ó¦·½³ĢŹ½½ųŠŠ¼ĘĖć£ŗ
5Fe2++MnO4-+8H+ØT5Fe3++Mn2++4H2O
5 1
n£ØFe2+£© 0.01000mol/L”Į0.0400L
¼ĘĖćµĆµ½£»n£ØFe2+£©=0.002mol£»
Ōņ250mLČÜŅŗÖŠŗ¬Fe2+=0.002mol”Į$\frac{250}{25}$=0.02mol£»
FeSO4•7H2OĪļÖŹµÄĮæĪŖ0.02mol£¬ÖŹĮæ=0.02mol”Į278g/mol=5.56g£»
ÖŹĮæ·ÖŹż=$\frac{5.56g}{5.7g}$”Į100%=97.54%£¬
¹Ź“š°øĪŖ£ŗ97.54%£®
µćĘĄ ±¾Ģāæ¼²éĮĖµĪ¶ØÖÕµćµÄČ·¶Ø”¢Ąė×Ó·½³ĢŹ½µÄ¼ĘĖć£¬Ć÷Č·Ńõ»Æ»¹Ō·“Ó¦ŗĶĄė×Ó·½³ĢŹ½ŹĒ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£¬×öĪÄ×ÖŠšŹöĢāÄæ“šĢāŹ±ŅŖĒŠÖŠŅŖµć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ö²ŹĒŅ»ÖÖ·ÖÉ¢Ļµ£¬·ÖÉ¢ÖŹŹĒ¹ĢĢå | |
| B£® | ĪķŹĒŅ»ÖÖ·ÖÉ¢Ļµ£¬·ÖÉ¢¼ĮŹĒĘųĢå | |
| C£® | ö²ŹōÓŚ½ŗĢå·ÖÉ¢Ļµ | |
| D£® | ¼õÉŁÉś²śÉś»īÖŠ²śÉśµÄŃļ³¾æÉŅŌ¼õÉŁĪķö²ĢģĘųµÄŠĪ³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬Į½ÖÖĘųĢåµÄĢå»żÖ®±ČµČӌĦ¶ūÖŹĮæÖ®±Č | |
| B£® | Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬Į½ÖÖĘųĢåµÄĪļÖŹµÄĮæÖ®±ČµČÓŚĆܶČÖ®±Č | |
| C£® | Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬Į½ÖÖĘųĢåµÄĦ¶ūÖŹĮæÖ®±ČµČÓŚĆܶČÖ®±Č | |
| D£® | Ķ¬ĪĀĶ¬ČŻĻĀ£¬Į½ÖÖĘųĢåµÄÖŹĮæÖ®±ČµČÓŚŃ¹ĒæÖ®±Č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×ĶéµÄČ¼ÉÕČČĪŖ890.3 kJmor-1£¬Ōņ¼×ĶéČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖCH4£Øg£©+202 £Øg£©ØTC02 £Øg£©+2H20£Øg£©”÷H=-890.3kJ mol-1 | |
| B£® | 500 V”¢30MPaĻĀ£¬½«0.5molN2ŗĶ1.5 molH2ÖĆÓŚĆܱյÄČŻĘ÷ÖŠ³ä·Ö·“Ӧɜ³É NH3£Øg£©£¬·ÅČČ19.3kJ£¬ĘäČČ»Æѧ·½³ĢŹ½ĪŖ N2£Øg£©+3H2 £Øg£©$?_{500”ę”¢30Mp}^{“߻ƼĮ}$2NH3£Øg£©”÷H=-38.6 kJmol-1 | |
| C£® | Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬µČĪļÖŹµÄĮæµÄH2Óė×ćĮæµÄC12ŌŚ¹āÕÕŗĶµćČ¼Ģõ¼žĻĀ³ä·Ö·“Ó¦£¬Ėł²śÉśµÄČČĮæĻąĶ¬ | |
| D£® | ŅŃÖŖÖŠŗĶČČĪŖ57.3 kJ/mol£¬ŌņĻ”ĮņĖįÓėĒāŃõ»Æ±µČÜŅŗ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ 2H+£Øaq£©+SO42-£Øaq£©+Ba2+£Øaq£©+20H-£Øaq£©=BaS04 £Øs£©+2H20£Øl£©”÷H=-57.3kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
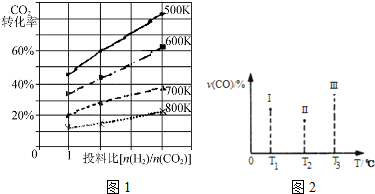
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
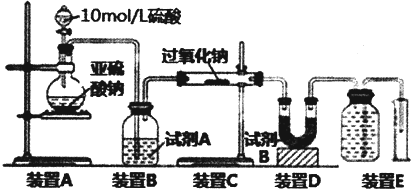
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČ»ÆÄĘĖ®ČÜŅŗŌŚµēĮ÷µÄ×÷ÓĆĻĀµēĄė³öNa+ŗĶCl- | |
| B£® | ĮņĖį±µÄŃČÜÓŚĖ®£¬µ«ĮņĖį±µŹōÓŚĒæµē½āÖŹ | |
| C£® | ¶žŃõ»ÆĢ¼ČÜÓŚĖ®Äܲæ·ÖµēĄė£¬¹Ź¶žŃõ»ÆĢ¼ŹōÓŚČõµē½āÖŹ | |
| D£® | ĮņĖįĒāÄĘŌŚĖ®ÖŠµÄµēĄė·½³ĢŹ½æɱķŹ¾ĪŖNaHSO4ØTNa++HSO4- |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com