
(8��)ʵ�����ﳣ��Ũ������������̷�Ӧ����ȡ��������������Ӧ�Ļ�ѧ����ʽΪ��MnO2��4HCl(Ũ) MnCl2��Cl2����2H2O��ȡһ������Ũ����ʹ����������̷�����Ӧ�������������ڱ�״���µ����Ϊ22��4 L��
MnCl2��Cl2����2H2O��ȡһ������Ũ����ʹ����������̷�����Ӧ�������������ڱ�״���µ����Ϊ22��4 L��
��ش��������⣺
��1��д���÷�Ӧ�����ӷ�Ӧ����ʽ_____________________________________��
��2���μӷ�Ӧ�Ķ������̵�����Ϊ____________��
��3����Ӧ�б�������HCl�����ʵ���Ϊ ____________��
��4��ʵ���ұ��õ�Ũ������������Ϊ36.5%���ܶ�Ϊ1.19g��cm��3��Ϊʹ�÷��㣬��������Ũ����
�����ʵ���Ũ��______________��
��1��MnO2��2Cl����4H��===Mn2����Cl2����2H2O ��2��87 g��3��2 mol ��4��11.9 mol��L��1
��������
�����������1�� ���ݻ�ѧ����ʽ�����ӷ���ʽΪ��MnO2��2Cl����4H�� Mn2����Cl2����2H2O��2�����������Ϊ22��4 L ��Cl2�������ʵ���Ϊ��n=22.4L��22.4L/mol=1mol,��������̵���������Ϊ�����У�
Mn2����Cl2����2H2O��2�����������Ϊ22��4 L ��Cl2�������ʵ���Ϊ��n=22.4L��22.4L/mol=1mol,��������̵���������Ϊ�����У�
MnO2��4HCl(Ũ)  MnCl2��Cl2����2H2O
MnCl2��Cl2����2H2O
1 1
n 1mol ��n=1mol��MnO2����Ϊm=1mol��87g/mol=87g��
��3����Ӧ������1mol Cl2Ҫ����4molHCl,��ֻ��һ���HCl����ԭ���� Ϊ2 mol ����4�� ���� c=1000��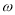 /M=1000��1.19g��cm��3��36.5%��36��5g/mol=11.9 mol��L��1
/M=1000��1.19g��cm��3��36.5%��36��5g/mol=11.9 mol��L��1
���㣺������ԭ��Ӧ�Ļ���������й����ʵ������㡣


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ���ָ���1�·�ͳһ�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ������Ԥ����ȷ����

A��ʵ��I�����ã��ϲ���Һ��ɫ���ֲ���
B��ʵ��II������KMnO4��Һ�г������ݣ�����ɫ����ȥ
C��ʵ��III����ϡHNO3��ҺƬ�̣���Һ�������ݲ��������ƿ��ʼ�ձ�����ɫ
D��ʵ��IV�����������Һ�����ɫ��ֹͣ���ȣ�������ͨ����ϵʱ�����ЧӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ����Ԫ��ģ����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����
A��16 g CH4��18 g NH4���������������
B��32S��33S�ĺ����������ȣ���ͬһ�ֺ���
C��������ȡ�������ȵ�N2��C2H4�ķ��������
D��ͬ��������֮���ת���������仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ��������ѧ�ڸ������Ĵ��¿����ۻ�ѧ�Ծ��������棩 ���ͣ��ƶ���
��13�֣���ͼ��A��K�ֱ�����йط�Ӧ��һ�ַ�Ӧ������������A��C��F��K�ǹ��塣��֪A��һ�ֲ�������Ԫ�ص��Σ����ȷֽ�õ����ֲ������ʵ���֮��Ϊ2�U1�U1��A���Ⱥ����ɵĻ��������ͨ����ʯ�ң�ֻʣ������B��BΪ��ɫ�д̼�����ζ�����壩����ͨ��Ũ������ֻʣ������D��DΪ��ɫ��ζ���壩��CΪ����ɫ���塣�����ʼ��ת����ϵ����ͼ��ʾ��

��ش�
��1��D�л�ѧ��������Ϊ________��C�ĵ���ʽ ��B�Ŀռ乹��Ϊ_________��
��2��д��A����Һ������NaOH��Һ��Ӧ�����ӷ���ʽ ��
��3��д��J��K��Ӧ�Ļ�ѧ����ʽ ��
��4���ڱ�״����4��48L��H��Iǡ�ñ�100mlNaOH��Һ��ȫ���գ�����NaOH��Һ�����ʵ���Ũ��
Ϊ mol��L��1��
��5����ҵβ���к��и��ֵ����������Ҫ��NO��NO2,��ʾΪNOx��,NOx�����صĴ�����Ⱦ��,������Щ��������֮һ��ͨ��������B,��Ӧ�������һ����ɫ��ζ�����塣д��NOx��B��Ӧ�Ļ�ѧ����ʽ______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ��������ѧ�ڸ������Ĵ��¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й������ʷ����˵����ȷ����
A����֬�����ࡢ�����ʾ�����Ȼ�߷��ӻ�����
B�����ȼ��顢����ϩ�����屽�Ӿ���±����
C��CaCl2���ռ�۱���ϩ��Ϊ������
D��ϡ���������ᡢ������Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014--2015����ʡ��һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���������ַ�����ȡ���������ú��Ȼ���146�˵�Ũ�����������Ķ������̷�Ӧ ����87�˶���������������Ũ���ᷴӦ������������
A���ڱȢٶ� B���ٱȢڶ� C��һ���� D�����Ƚ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014--2015����ʡ��һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��5mL 0��05 mo1/L��ij�����Ȼ�����Һ�У��μ�7��5 mL 0��1 mo1/L AgNO3��Һǡ����ȫ��Ӧ������Ȼ����н���Ԫ�صĻ��ϼ�Ϊ
A��+1 B��+2 C��+3 D��+4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ��һ1���¿���ѧ�Ծ��������棩 ���ͣ������
(8��)θ��(��Ҫ�ɷ�Ϊ����)�����dz�����θ�����ס���������ѧ�α�����������θ�����ij���θҩ�����������ǵ�˵��ժҪ��
�ף���1����ɫ�ᾧ״��ĩ���ɻ����ֽ⣻
��2��������ˮ��ˮ��Һ�������ԣ�
��3�����ἰ����ҩ�������������̼��
�ң���1����θ�����к����û������־ã���ά��3��4Сʱ��
��2�����������������������ϣ����б������á�
��3��������ϡ�������������Һ�С�
��1�������Ʋ⣬���к��е���Ҫ��ѧ�ɷ��� �����������ƣ������к��е���Ҫ��ѧ�ɷ��� ���ѧʽ����
��2����д�����к��е���Ҫ��ѧ�ɷ�����θ������Ӧ�Ļ�ѧ����ʽ�� ��
��3����д�����к��е���Ҫ��ѧ�ɷݷֱ���ϡ���������������Һ��Ӧ�����ӷ���ʽ�� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ�߶�1���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Ȼ�ѧ����ʽ��д��ȷ����(��H�ľ���ֵ����ȷ)
A��C(s)��1/2O2(g)��CO(g)����H����110.5kJ��mol��1��ȼ���ȣ�
B��2H2O(g)��2H2(g)��O2(g)����H����483.6 kJ��mol��1����Ӧ�ȣ�
C��C2H5OH��3O2��2CO2��3H2O����H����1368.8 kJ��mol��1����Ӧ�ȣ�
D��2NaOH(aq)��H2SO4(aq)��Na2SO4 (aq)��2H2O(l)����H����114.6 kJ��mol��1���к��ȣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com