
| A、10 mL |
| B、5 mL |
| C、大于5 mL |
| D、小于5 mL |
| n |
| c |
| 5×10-4mol |
| 0.1mol/L |


科目:高中化学 来源: 题型:

| A、该可逆反应的化学方程式为X(g)+Y(g)?2Z(g) |
| B、该可逆反应的△H>0 |
| C、图1中反应达到平衡时,X的转化率为16.7% |
| D、T1℃时,若该反应的平衡常数K=50,则T1>T0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加稀盐酸产生无色无味气体,将气体通入澄清石灰水,石灰水变浑浊,原溶液可能含CO32- |
| B、加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀消失,原溶液一定含有SO42- |
| C、加入AgNO3溶液有白色沉淀产生,原溶液一定含有Cl- |
| D、加入Na2CO3溶液有白色沉淀产生,再加盐酸,白色沉淀消失,原溶液中一定含有Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、降低温度 |
| B、增大压强 |
| C、升高温度同时充入N2 |
| D、及时将C02和N2从反应体系中移走 |
查看答案和解析>>
科目:高中化学 来源: 题型:
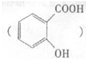 可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解.写出水杨酸与小苏打反应的化学方程式:
可导致患者出现头痛、恶心等症状,需静脉注射小苏打(NaHCO3)溶液,利用小苏打与水杨酸分子中的羧基反应生成水杨酸钠,使症状缓解.写出水杨酸与小苏打反应的化学方程式:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com