
【题目】在25 ℃、101 kPa条件下,将15 L O2通入10 L CO和H2的混合气体中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15 L,则原CO和H2的混合气体中V(CO)=________ L,V(H2)=________ L。
(2)若剩余气体的体积为a L,则原CO和H2的混合气体中V(CO)∶V(H2)=________。
(3)若剩余气体的体积为a L,则a的取值范围是________。
【答案】55![]() 10<a<20
10<a<20
【解析】
试题(1)设一氧化碳的体积为x,则氢气的体积为10-x,根据化学方程式
2CO+O2=2CO2 2H2+O2=2H2O
2 1 2 2 1
X 0.5x x 10-x (10-x)/2
依题意,x+15-0.5x-(10-x)/2=15,则x=5升,所以氢气的体积为10-5=5升;
(2)依题意,x+15-0.5x-(10-x)/2=a,x=a-10,则氢气的体积为10-(a-10)=20-a,所以二者的体积比为(a-10):(20-a)。(3)一氧化碳的体积应该大于0,所以a-10>0,则a>10,氢气的体积应大于0,所以20-a>0,所以有a<20,所以10<a<20。


科目:高中化学 来源: 题型:
【题目】25 ℃时,体积均为20 mL、浓度均为0.1 mol L-1的两种酸HX、HY分别与0.1 mol L-1的NaOH溶液反应,所加NaOH溶液体积与反应后溶液的-pH的关系如图所示。下列叙述正确的是
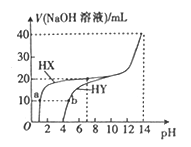
A. a点c(X-)>b点c(Y-) B. HX发生反应的离子方程式为HX+OH-=X-+H2O
C. Ka(HY)的数量级约为10-3 D. pH=7时,两种反应后的溶液中c(Y-)>c(X-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米铜是一种性能优异的超导材料,以辉铜矿(主要成分为Cu2S)为原料制备纳米铜粉的工艺流程如图1所示。

(1)用黄铜矿(主要成分为CuFeS2)、废铜渣和稀硫酸共同作用可获得较纯净的Cu2S,其原理如图2所示,该反应的离子方程式为__________________。
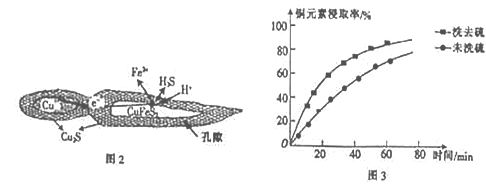
(2)从辉铜矿中浸取铜元素时,可用FeCl3溶液作浸取剂。
①反应:Cu2S+4FeCl3=2CuCl2+4FeCl2+S,每生成1molCuCl2,反应中转移电子的物质的量为______;浸取时,在有氧环境下可维持Fe2+较高浓度,有关反应的离子方程式为________。
②浸取过程中加入洗涤剂溶解硫时,铜元素浸取率的变化如图3 所示,未洗硫时铜元素浸取率较低,其原因是_____________________。
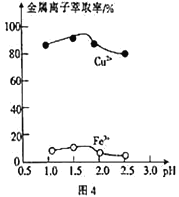
(3)“萃取”时,两种金属离子萃取率与pH的关系如图4 所示,当pH>1.7时,pH越大,金属离子萃取率越低,其中Fe2+萃取率降低的原因是_________________。
(4)用“反萃取”得到的CuSO4溶液制备纳米铜粉时,该反应中还原产物与氧化产物的质量之比为_______________。
(5)在萃取后的“水相”中加入适量氨水,静置,再经过滤、_____、干燥、_____等操作可得到Fe2O3产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷中混有乙烯,欲除乙烯得到纯净的甲烷,可依次将其通过下列哪组试剂的洗气瓶
A.澄清石灰水,浓H2SO4B.溴水,NaOH溶液,浓H2SO4
C.酸性高锰酸钾溶液,浓H2SO4D.浓H2SO4,酸性高锰酸钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应最后能产生沉淀的是( )
A.向AlCl3溶液中加过量的NaOH溶液
B.向NaAlO2溶液中加过量的盐酸
C.向AlCl3溶液中通入过量的CO2
D.向NaAlO2溶液中通入过量的CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个固定体积的密闭容器中,加入4molA和2molB发生反应:2A(g)+B(g)![]() 3C(g)+D(g)达到平衡时,C的浓度为Wmol/L,若维持容器体积和温度不变,按下列四种方法改变起始物质,达到平衡后,C的浓度仍为Wmol/L的是( )
3C(g)+D(g)达到平衡时,C的浓度为Wmol/L,若维持容器体积和温度不变,按下列四种方法改变起始物质,达到平衡后,C的浓度仍为Wmol/L的是( )
A. 4molA+2molB
B. 2molA+1molB+3molC+1molD
C. 3molC+1molD+1molB
D. 3molC+1molD
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】混合动力车在刹车和下坡时处于充电状态;上坡或加速时,电动机提供辅助推动力,降低了汽油的消耗。该车一般使用的是镍氢电池采用镍的化合物和储氢金属(以M表示)为两电极材料,碱液(主要为KOH)电解液。镍氢电池充放电原理如图,其总反应式为:H2+2NiOOH = 2Ni(OH)2 下列有关判断正确的是( )

A. 在上坡或加速时,溶液中的K+向甲电极迁移
B. 在刹车和下坡时,甲电极的电极反应式为:2 H2O+2e- H2↑+2OH-
C. 在上坡或加速时,乙电极周围溶液的pH将减小
D. 在刹车和下坡时,乙电极增重
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com