
A.与AlCl3溶液发生反应的离子方程式为Al3++3OH-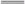 Al(OH)3↓ Al(OH)3↓ |
| B.其溶液的pH=13 |
| C.用适量水稀释后,NH3·H2O电离度和溶液pH都增大 |
| D.加水稀释后,溶液中c(NH4 +)·c(OH-)变小 |
科目:高中化学 来源:不详 题型:单选题
| A.常温下,某溶液中由水电离出来的c(H+)=1×10―amol·L―1,若a<7,则该溶液可能为NaHSO4溶液 |
| B.中和同体积、同pH的硫酸、盐酸和醋酸所需相同浓度的NaOH溶液的体积关系:V(硫酸)>V(盐酸) >V(醋酸) |
| C.pH相等的①CH3COONa②C6H5ONa③NaHCO3溶液中,c(Na+)大小关系:②<③<① |
| D.已知Ag2CrO4的Ksp为1.12×10-12,将等体积的1×10-4mol·L-1的AgNO3溶液和1×10-4mol·L-1K2CrO4溶液混合,会有Ag2CrO4沉淀产生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.滴入酚酞溶液显红色的溶液中:K+、Na+、Cu2+、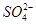 |
B.加入过量NaOH溶液或少量稀H2SO4时,都能产生白色沉淀的溶液:Al3+、Ba2+、Cl-、 |
C.水电离产生的c(H+)=10-13mol·L-1的溶液中:Na+、Cl-、 、 、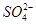 |
D.0.1 mol·L-1HNO3溶液中:Mg2+、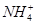 、Fe2+、Cl- 、Fe2+、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CH3COO-+H+,下列关于醋酸说法错误的是
CH3COO-+H+,下列关于醋酸说法错误的是| A.加水稀释,所有离子浓度都减少 |
| B.加入少量固体CH3COONa,平衡向逆方向移动,c(H+)减少 |
| C.升高温度促进了醋酸的电离,Ka增大。 |
| D.醋酸溶液的导电性不一定比盐酸要弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 实验 编号 | HA的物质的量浓度(mol·L-1) | NaOH的物质的量浓度(mol·L-1) | 混合后溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
 H++B2-
H++B2-查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
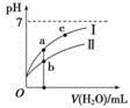
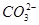
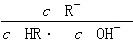 相等(HR代表CH3COOH或HClO)
相等(HR代表CH3COOH或HClO)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H++A2-
H++A2-查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1:4.3×10-7 K2:5.6×10-11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com