
(14分)A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的最外层电子数是次外层电子数2倍,B是短周期中金属性最强的元素,C是同周期中阳离子半径最小的元素,D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,E的最外层电子数与内层电子数之比为3﹕5。请回答:
(1)D的元素符号为 。
(2)F在元素周期表中的位置 。
(3)用电子式表示元素B与元素F形成的化合物: 。
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关的化学方程式为 、 。
(5)工业上将干燥的F单质通入熔融的E单质中可制得化合物E2F2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为 。
(6)某混合物的稀溶液中,只可能含有B、C、F构成的简单离子或A、E的最高价氧化物对应水化物所电离出来的阴离子。现分别取一定体积的该溶液进行实验。两次每次取200.00mL进行实验。
实验1:取2mL溶液,向其中加入AgNO3溶液有沉淀产生;
实验2:取200mL溶液,向其中加入足量BaCl2溶液后,得干燥沉淀12.54g,沉淀经足量盐酸洗涤、干燥后,剩余4.66g。请回答:
①根据以上实验,不能判断是否存在的离子有 。
② B的简单离子是否存在 ;若存在,浓度至少为 mol/L(若不存在,则不必回答第二问)。
(1)Si (1分)(2)第3周期,VIIA(2分)(3)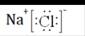 (1分)
(1分)
(4)2Na2O2 + 2H2O=4NaOH + O2↑(2分) 2Al+ 2NaOH + 2H2O=2NaAlO2 +3H2↑(2分)
(5)2S2Cl2 + 2H2O ="=" 3S + SO2↑+ 4HCl (2分)
(6) ①Cl- HCO3- (各1分,共2分)② 存在,0.6 (2分)
解析试题分析:A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的最外层电子数是次外层电子数2倍,则A是第二周期元素,因此A是碳元素。B是短周期中金属性最强的元素,则B是钠元素。C是同周期中阳离子半径最小的元素,原子序数大于钠,则C是铝元素。D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,所以D是硅元素。E的最外层电子数与内层电子数之比为3﹕5,则E是硫元素,所以F是氯元素。
(1)根据以上分析可知D的元素符号为Si。
(2)F的原子序数是17,在元素周期表中的位置第三周期第VIIA族。
(3)氯化钠是离子化合物,电子式为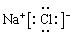 。
。
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,这说明钠与氧气的产物是过氧化钠,过氧化钠溶于水生成氢氧化钠和氧气。氢氧化钠与铝反应生成偏氯酸钠和氢气,有关的化学方程式为2Na2O2 + 2H2O=4NaOH + O2↑、2Al+ 2NaOH + 2H2O=2NaAlO2 +3H2↑。
(5)工业上将干燥的F单质通入熔融的E单质中可制得化合物E2F2,该物质可与水反应生成一种能使品红溶液褪色的气体,该气体是SO2。0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变。在S2Cl2中S元素的化合价+1价,所以化合价发生变化的元素是S,氧化产物是SO2,还原产物是S,该反应的化学方程式为2S2Cl2 + 2H2O=3S + SO2↑+ 4HCl。
(6)实验1:取2mL溶液,向其中加入AgNO3溶液有沉淀产生,说明含有氯离子或硫酸根离子或碳酸根离子;实验2:取200mL溶液,向其中加入足量BaCl2溶液后,得干燥沉淀12.54g,沉淀经足量盐酸洗涤、干燥后,剩余4.66g,这说明4.66g沉淀是;硫酸钡,物质的量是0.02mol,碳酸钡的质量是12.54g—4.66g=7.88g,物质的量是0.04mol,一定含有硫酸根和碳酸根,则一定没有铝离子。根据溶液的电中性可知一定含有钠离子。
①根据以上分析可知,不能判断是否存在的离子有Cl-、HCO3-。
②根据以上分析可知,钠离子一定存在。由于硫酸根和碳酸根的浓度分别是0.1mol/L、0.2mol/L,而氯离子与碳酸氢根离子不能确定,所以根据电荷守恒可知钠离子浓度至少为0.1mol/L×2+0.2mol/L×2=0.6mol/L。
考点:考查元素推断的有关应用


科目:高中化学 来源: 题型:单选题
下列物质组合中,既能和酸反应又能和碱反应的化合物是
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3
| A.①②③④ | B.②③④ | C.①③④ | D.①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
14分)在下图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,F在D中燃烧发出苍白色火焰。H可用于制造光导纤维,J是一种乳白色凝胶状沉淀。(部分生成物和部分反应条件未列出) 请回答下列问题:
(1)形成单质D的元素在周期表中的位置
(2)形成C、D、F单质的元素半径由大到小的顺序(填写元素符号)
(3)C长期暴露在空气中,最终产物是
(4)H在高温下与碳反应方程式为 ,若转移4mol电子参加反应的碳为 mol。
(5)写出反应①的离子方程式
(6)写出反应②的化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(15分)材料科学是近年来与化学有关的科学研究热点。某新型无机非金属材料K由两种非金属元素组成。它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特征。它是以中学化学中常见物质为原料来生产的。下图虚线框内的其它转化是为探究C的组成而设。G、F、H均为难溶于水的白色固体;图中C、H、K均为含A元素。其余物质均为中学化学中常见物质。
请回答下列问题:
(1)实验室通常用MnO2制取气体B,发生该反应的化学方程式为 ,为防止气体B污染环境通常
用 (填化学式)溶液吸收,反应的离子方程式为
(2)化合物H与碳混合加强热可制得单质A,该反应中氧化剂与还原剂的物质的量比为
(3)写出反应③的化学方程式3D==K+8X↑,K的化学式为 ,X的化学式为 。
(4)K抗腐蚀能力很强,但易被氢氟酸腐蚀,K与氢氟酸反应生成一种气体和一种盐,此盐中存在的化学键类型有 。
(5)写出反应②的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(本题包括2部分,共14分)
Ⅰ、(8分)X、Y、Z、W均为短周期元素组成的单质或化合物。在一定条件下有如下转化关系:X+Y→Z+W
(1)若构成X的阳、阴离子个数比为1︰2,且构成X的阳、阴离子中分别含有18个和10个电子,构成Z的阴、阳离子中均含有10个电子。则Z的电子式为 。
(2)若X、Y、Z、W四种物质均为分子,且X分子中含18个电子,Y、Z分子中均含有10个电子,单质W分子中含有16个电子。则此化学反应的类型为 。
(3)若X、W均为单质,Y、Z均为氧化物且Y、Z中氧的质量分数分别为50%和40%。则该反应的化学方程式为 。
(4)若X、Y、Z、W均为非金属氧化物,X的式量比Z的式量小16,Y的式量比W的式量大16,Y是光化学烟雾的主要“元凶”,则该反应的化学方程式为 。
Ⅱ、(6分)我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图:
请根据以上信息回答下列问题:
(1)写出N的化学式和B的名称:N 、B 。
(2)写出反应②的化学方程式并用双线桥表示电子转移情况:
(3)写出反应③的离子方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车倍受青睐。我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,并加快向产业化的目标迈进。氢能具有的优点包括
①原料来源广 ②易燃烧、热值高 ③储存方便 ④制备工艺廉价易行
| A.①② | B.①③ | C.③④ | D.②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关能量转换的说法正确的是
| A.煤燃烧是热能转化为化学能的过程 |
| B.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能 |
| C.动物体内葡萄糖被氧化是热能转变成生物能的过程 |
| D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com