
| 2 |
| 3 |
c(N
| ||
| c(OH-) |
| 2 |
| 3 |
| m |
| V |
| 10-3×10-3 |
| 0.1 |
c(N
| ||
| c(OH-) |


 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源:不详 题型:填空题
 2SO3(气),若在同温同压下测得反应前后混合气体的密度比为0.9:1。则反应掉的SO2是原有SO2的___________%。
2SO3(气),若在同温同压下测得反应前后混合气体的密度比为0.9:1。则反应掉的SO2是原有SO2的___________%。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.⑤⑥⑧ | B.②⑤⑧ | C.①③④ | D.②④⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.容器中的总压强不随时间的变化而变化 |
| B.单位时间内有nmolA2生成同时就有nmolB2生成 |
| C.单位时间内有nmolA2生成同时就有2nmolAB生成 |
| D.单位时间内有nmolB2生成同时就有2nmolAB分解 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.混合气体的颜色变浅 |
| B.单位时间内生成2nmolNO同时生成2nmolNO2 |
| C.混合气中NO2、NO、O2物质的量之比为2:2:1 |
| D.混合气体的密度不再变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应停止了 | B.容器内气体颜色不变 |
| C.容器内气体总质量不变 | D.容器内气体密度不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
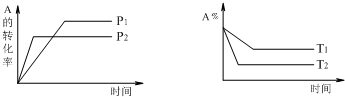
| A.a+b<c+d;正反应吸热 | B.a+b>c+d;正反应放热 |
| C.a+b<c+d;正反应放热 | D.a+b>c+d;正反应吸热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com