
| A. | ①② | B. | ①③ | C. | ①②④ | D. | ①②③④ |
分析 ①活泼的金属易与水反应,不能作电极;
②根据原电池的构成条件分析;
③原电池是将化学能转化为电能的装置;
④以锌、铜为电极,在稀硫酸溶液中构成原电池,负极反应式为Zn-2e-═Zn2+.
解答 解:①活泼的金属易与水反应,不能作电极,故错误;
③原电池的构成条件①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,若有活泼性不同的两种金属电极、有电解质溶液、导线,如果不能自发发生氧化还原反应,则不能形成原电池,故错误;
③原电池反应中能自发的进行氧化还原反应,是将化学能转化为电能的装置,故正确;
④以锌、铜为电极,在稀硫酸溶液中构成原电池,负极反应式为Zn-2e-═Zn2+,而不是正极,正极是2H++2e-=H2↑,故错误;
故选C.
点评 本题考查的内容是高考中的常见考点,属于基础性试题的考查,难度不大,明确原电池的工作原理、构成条件是答题的关键.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
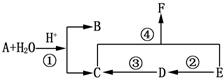
 .
.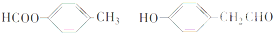 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过植物的光合作用,太阳能转化为热能 | |
| B. | 使用电炉加热食物,将电能转化为化学能 | |
| C. | 生物体内化学变化的过程在能量转化上比在体外发生的一些能量转化更为合理、有效 | |
| D. | 燃料燃烧,只是将化学能转化为热能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
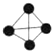 ),已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量,根据以上信息和数据,下列说法正确的是( )
),已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量,根据以上信息和数据,下列说法正确的是( )| A. | 14N2与15N2互为同位素,N4与N2互为同素异形体 | |
| B. | N4属于一种新型的化合物 | |
| C. | 14N与15N化学性质不相同 | |
| D. | 1mol N4气体完全转变为N2将放出882kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何可逆反应都有一定的限度 | |
| B. | 化学反应的限度是不可改变的 | |
| C. | 化学反应达到限度时,各物质的浓度不再改变 | |
| D. | 化学反应达到限度时,正逆反应速率相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com