
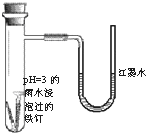
 (2011?朝阳区一模)如图是探究铁发生腐蚀的装置图.发现开始时U型管左端红墨水水柱下降,一段时间后U型管左端红墨水水柱又上升.下列说法不正确的是( )
(2011?朝阳区一模)如图是探究铁发生腐蚀的装置图.发现开始时U型管左端红墨水水柱下降,一段时间后U型管左端红墨水水柱又上升.下列说法不正确的是( )

科目:高中化学 来源: 题型:
(2011?朝阳区一模)常温下,有下列四种溶液:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 水 |
| 自然风干 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com