
【题目】做完海带提碘实验后,实验室得到了含碘废液(含水、CCl4、可能含I2、I—、IO3—的一种或几种),为测定废液中碘的存在形式,并回收废液中的碘和CCl4,设计了如下实验方案。完成下列填空:
Ⅰ.判断废液中碘的存在形式(已知:5SO32—+ 2IO3—+2H+→I2+5SO42—+H2O)
实验中可供选择的试剂是:稀盐酸、淀粉溶液、氯化铁溶液、亚硫酸钠溶液
(1)观察废液,废液分为上下两次,有机层在____层(填“上”或“下”),呈____色。
(2)从废液中取少量水层溶液(pH≈8),滴加淀粉溶液,变为蓝色,该废水中含I2;另从废液中取适量水层溶液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有I2存在;取________ ,该废水中含有I—;取______,该废水中不含IO3—。
Ⅱ.回收该废液中的碘和CCl4
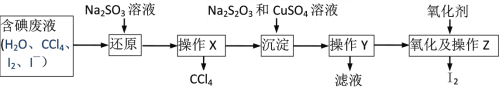
(3)向含碘废液中加入稍过量的Na2SO3溶液,将I2还原为I—,该操作的目的是_______;操作X名称是________。
(4)Na2S2O3、CuSO4溶液和I—反应生成CuI沉淀和Na2S4O6溶液,已知该含碘废液中碘元素的含量为10.33g/L,若回收500mL该含碘废液中的碘,则至少需要2mol/L的硫酸铜溶液_______mL。
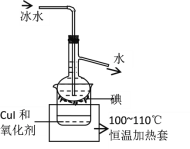
(5)将CuI转移入烧杯中,加入氧化剂在如图所示的装置中反应,一段时间后在蒸馏烧瓶底得到____色的固体碘。H2O2是一种性能优良的绿色氧化剂可将CuI氧化为I2,本实验不选用H2O2,可能的原因是_______。
【答案】下 紫色(或紫红色) 取除去I2的水层溶液少许,加入1~2mL淀粉溶液,加盐酸酸化,滴加氯化铁溶液,溶液变蓝 另取除去I2的水层溶液少许,加入1~2mL淀粉溶液,加盐酸酸化,滴加亚硫酸钠溶液,溶液不变蓝 使四氯化碳中的碘进入水层 分液 20.33 紫黑色 本实验氧化和升华是同时进行的,H2O2温度较高时易分解(合理即得分)
【解析】
Ⅰ、![]() 废液中的碘和
废液中的碘和![]() ,在水中分层,有机层在水溶液下层,碘单质溶于四氯化碳呈紫色;
,在水中分层,有机层在水溶液下层,碘单质溶于四氯化碳呈紫色;
![]() 碘离子具有还原性,能被氧化剂氧化生成碘,碘酸根离子具有氧化性,能被还原剂还原生成碘,碘遇淀粉试液变蓝色,所以其检验方法为:从水层取少量溶液,加入
碘离子具有还原性,能被氧化剂氧化生成碘,碘酸根离子具有氧化性,能被还原剂还原生成碘,碘遇淀粉试液变蓝色,所以其检验方法为:从水层取少量溶液,加入![]() 淀粉溶液,加入盐酸酸化,滴加
淀粉溶液,加入盐酸酸化,滴加![]() 溶液,
溶液,![]() ,若溶液变蓝色,说明废水中含有
,若溶液变蓝色,说明废水中含有![]() ,否则不含
,否则不含![]() ;另从水层取少量溶液,加入
;另从水层取少量溶液,加入![]() 淀粉试液,加盐酸酸化,滴加
淀粉试液,加盐酸酸化,滴加![]() 溶液,发生
溶液,发生![]() ,若溶液变蓝色,说明废水中含有
,若溶液变蓝色,说明废水中含有![]() ,否则不含
,否则不含![]() ;
;
Ⅱ、![]() 向含碘废液中加入稍过量的
向含碘废液中加入稍过量的![]() 溶液,将废液中的
溶液,将废液中的![]() 还原为
还原为![]() ,四氯化碳属于有机物,水属于无机物,二者不互溶,分离互不相溶的液体采用分液的方法分离,所以分离出四氯化碳采用分液的方法;
,四氯化碳属于有机物,水属于无机物,二者不互溶,分离互不相溶的液体采用分液的方法分离,所以分离出四氯化碳采用分液的方法;
![]() ,结合碘元素守恒和化学方程式中定量关系计算得到;
,结合碘元素守恒和化学方程式中定量关系计算得到;
![]() 碘单质是紫黑色固体,过氧化氢受热易分解。
碘单质是紫黑色固体,过氧化氢受热易分解。
Ⅰ、![]() 废液中的碘和
废液中的碘和![]() ,在水中分层,有机层在水溶液下层,碘单质溶于四氯化碳呈紫色,故答案为:下;紫;
,在水中分层,有机层在水溶液下层,碘单质溶于四氯化碳呈紫色,故答案为:下;紫;
![]() 碘离子具有还原性,能被氧化剂氧化生成碘,碘酸根离子具有氧化性,能被还原剂还原生成碘,碘遇淀粉试液变蓝色,所以其检验方法为从水层取少量溶液,加入
碘离子具有还原性,能被氧化剂氧化生成碘,碘酸根离子具有氧化性,能被还原剂还原生成碘,碘遇淀粉试液变蓝色,所以其检验方法为从水层取少量溶液,加入![]() 淀粉溶液,加入盐酸酸化,滴加
淀粉溶液,加入盐酸酸化,滴加![]() 溶液,
溶液,![]() ,若溶液变蓝色,说明废水中含有
,若溶液变蓝色,说明废水中含有![]() ,否则不含
,否则不含![]() ;另从水层取少量溶液,加入
;另从水层取少量溶液,加入![]() 淀粉试液,加盐酸酸化,滴加
淀粉试液,加盐酸酸化,滴加![]() 溶液,
溶液,![]() ,若溶液变蓝色,说明废水中含有
,若溶液变蓝色,说明废水中含有![]() ,否则不含
,否则不含![]() ,故答案为:
,故答案为:![]() 的水层溶液少许,加入
的水层溶液少许,加入![]() 淀粉溶液,加盐酸酸化,滴加氯化铁溶液,溶液变蓝;另取除去
淀粉溶液,加盐酸酸化,滴加氯化铁溶液,溶液变蓝;另取除去![]() 的水层溶液少许,加入
的水层溶液少许,加入![]() 淀粉溶液,加盐酸酸化,滴加亚硫酸钠溶液,溶液不变蓝;
淀粉溶液,加盐酸酸化,滴加亚硫酸钠溶液,溶液不变蓝;
Ⅱ、![]() 向含碘废液中加入稍过量的
向含碘废液中加入稍过量的![]() 溶液,将废液中的
溶液,将废液中的![]() 还原为
还原为![]() ,其离子方程式为
,其离子方程式为![]() ,四氯化碳属于有机物,水属于无机物,二者不互溶,分离互不相溶的液体采用分液的方法分离,所以分离出四氯化碳采用分液的方法;故答案为:四氯化碳中的碘进入水层;分液;
,四氯化碳属于有机物,水属于无机物,二者不互溶,分离互不相溶的液体采用分液的方法分离,所以分离出四氯化碳采用分液的方法;故答案为:四氯化碳中的碘进入水层;分液;
![]() 已知该含碘废液中碘元素的含量为
已知该含碘废液中碘元素的含量为![]() ,若回收500mL该含碘废液中的碘,含碘元素质量
,若回收500mL该含碘废液中的碘,含碘元素质量![]() ,物质的量
,物质的量![]() ,
,![]() ,依据反应定量关系得到,至少需要
,依据反应定量关系得到,至少需要![]() 的硫酸铜溶液体积
的硫酸铜溶液体积![]() ;故答案为:
;故答案为:![]() ;
;
![]() 将CuI转移入烧杯中,加入氧化剂在如图2所示的装置中反应,一段时间后在蒸馏烧瓶底得到紫红色固体碘单质,
将CuI转移入烧杯中,加入氧化剂在如图2所示的装置中反应,一段时间后在蒸馏烧瓶底得到紫红色固体碘单质,![]() 是一种性能优良的绿色氧化剂可将CuI氧化为
是一种性能优良的绿色氧化剂可将CuI氧化为![]() ,本实验不选用
,本实验不选用![]() ,可能的原因是过氧化氢易分解失去氧化性;故答案为:紫黑;过氧化氢易分解。
,可能的原因是过氧化氢易分解失去氧化性;故答案为:紫黑;过氧化氢易分解。


 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. ![]() 的一溴代物和
的一溴代物和![]() 的一溴代物都有4种(不考虑立体异构)
的一溴代物都有4种(不考虑立体异构)
B. CH3CH=CHCH3分子中的四个碳原子在同一直线上
C. 按系统命名法,化合物 的名称是2,3,4-三甲基-2-乙基戊烷
的名称是2,3,4-三甲基-2-乙基戊烷
D. 丙酸与甲酸甲酯互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯氧布洛芬是一种解热、阵痛、消炎药,其药效强于阿司匹林。可通过以下路线合成:
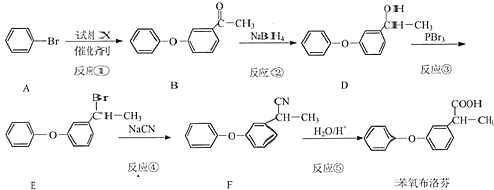
完成下列填空:
(1)反应①中加入试剂X的分子式为C8H8O2,X的结构简式为_______。
(2)反应①往往还需要加入KHCO3,加入KHCO3的目的是__________。
(3)在上述五步反应中,属于取代反应的是________(填序号)。
(4)B的一种同分异构体M满足下列条件:
Ⅰ.能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应。
Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环。则M的结构简式: ____。
(5)请根据上述路线中的相关信息并结合已有知识,写出以![]() 、CH2CHO。为原料制备
、CH2CHO。为原料制备![]() 的合成路线流程图(无机试剂任用)____。
的合成路线流程图(无机试剂任用)____。
合成路线流程图示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知如表数据。
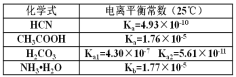
(1)25℃时,pH=11的NaCN溶液中水电离出的c(OH-)=_____molL-1。
(2)25℃时,等浓度的NaCN、Na2CO3溶液、CH3COONa三种溶液的pH值由大到小的顺序为_____。
(3)0.100molL-1NH4HCO3溶液中物质的量浓度最大的离子是_____(填化学式)。
(4)向NaCN溶液中通入少量CO2,所发生反应的化学方程式为_____。
(5)25℃1.10molL-1CH3COOH溶液中,CH3COOH的电离度约为_____。
(6)25℃时等体积等浓度的NaCl与NaCN两溶液中,离子总数NaCl_____NaCN(填“大于”、“小于”或“等于”);
(7)HCN与NaOH反应后的溶液中存在:c(Na+)=c(CN-),该溶液呈_____性(填“酸”“碱”或“中”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)将过量的氨水加入氯化铝溶液的离子方程式_____;
(2)浓硝酸久置后会略显黄色,可用方程式表示为_____;
(3)用KOH作电解质溶液,氢氧燃料电池负极反应式为_____;
(4)用方程式表示氯化铵溶液呈酸性原因_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是合成高活性、安全农药茚虫威的重要中间体。
已知:![]()
以化合物A为原料合成化合物F的流程如下:
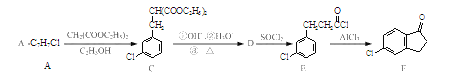
完成下列填空:
(1)写出反应A→B的化学方程式_________。
(2)写出化合物D中含氧官能团的名称_______;写出B→C的反应类型__________。
(3)某化合物是D的同分异构体,能使FeCl3溶液显紫色,且分子中只有3种不同化学环境的氢。写出该化合物的结构简式__________(任写一种)。
(4)E→F的转化中,会产生一种与F互为同分异构体且碳环上碳原子数目相同的副产物,其结构简式为________________。
(5)根据已有知识并结合所给信息,写出以化合物F和CH2(COOC2H5)2为有机反应原料制备![]() 的合成路线流程图(注明反应条件)_______。合成路线流程图示例如下:
的合成路线流程图(注明反应条件)_______。合成路线流程图示例如下:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据操作和现象所得出的结论正确的是( )
选项 | 实验操作及现象 | 实验结论 |
A | 向KI溶液中加入30%H2O2、稀硝酸及淀粉溶液,溶液变蓝 | H2O2氧化性比I2强 |
B | 向Na2CO3溶液中加稀硫酸将产生的气体通入硅酸钠溶液中产生白色沉淀 | 非金属性:S>C>Si |
C | 向某溶液中滴加稀NaOH溶液时,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 原溶液不含NH4+ |
D | 将BaSO4浸泡在饱和Na2CO3溶液中,一段时间后过滤并洗涤沉淀,向沉淀中加入稀盐酸,有气泡产生 | Ksp(BaSO4)>Ksp(BaCO3) |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物的命名及名称书写均正确的是
A.CH2Br-CH2Br 二溴乙烷
B.CH3CH(NH2)CH2COOH 3-氨基丁酸
C. 硬脂酸甘油脂
硬脂酸甘油脂
D. 2,2-二甲基-3-丁醇
2,2-二甲基-3-丁醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质为常见有机物:
①甲苯 ②1,3﹣丁二烯 ③直馏汽油 ④植物油
填空:
(1)既能使溴水因发生化学变化褪色,也能使酸性高锰酸钾褪色的烃是____(填编号);
(2)能和氢氧化钠溶液反应的是______(填编号),写出该反应产物之一与硝酸酯化的化学方程式______.
(3)已知:环己烯可以通过1,3﹣丁二烯与乙烯发生环化加成反应得到:
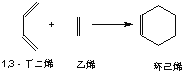
实验证明,下列反应中,反应物分子的环外双键比环内双键更容易被氧化:
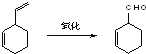
现仅以1,3﹣丁二烯为有机原料,无机试剂任选,按下列途径合成甲基环己烷:
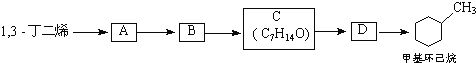
(a)写出结构简式:A______;B_____
(b)加氢后产物与甲基环己烷互为同系物的是_______
(c)1mol A与1mol HBr加成可以得到_____种产物.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com