
| A. | 碱性氧化物:Na2O、CaO、Al2O3、H2O | B. | 碱:NaOH、KOH、Ba(OH)2、Na2CO3 | ||
| C. | 氧化物:Fe2O3、NO、SO2、CuO | D. | 酸:H2SO4、HNO3、NaHSO4 |
分析 A.碱性氧化物是能和酸反应生成盐和水的氧化物;酸性氧化物是能和碱反应生成盐和水的氧化物;两性氧化物是不但可以和酸反应还可以和碱反应均生成盐和水的氧化物;既不能和酸、又不能和碱反应的氧化物为不成盐氧化物;
B.碱是指电离时产生的阴离子全部是氢氧根离子的化合物;
C.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素;
D.酸是指电离时产生的阳离子全部是氢离子的化合物,盐是指由金属离子和酸根离子组成的化合物.
解答 解:A.Na2O、CaO属于碱性氧化物,Al2O3、属于两性氧化物,H2O属于不成盐氧化物,故A错误;
B.NaOH、KOH、Ba(OH)2属于碱、Na2CO3属于盐,故B错误;
C.Fe2O3、NO、SO2、CuO都是由两种元素组成的化合物,且其中一种元素是氧元素,故C正确;
D.H2SO4、HNO3属于酸,NaHSO4属于硫酸的酸式盐,故D错误;
故选C.
点评 本题主要考查了物质的分类,掌握酸、碱、盐、氧化物的概念是解答的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | C3H8、C4H4、C4H6 | B. | CH4、C3H6、C2H2 | C. | C2H6、C3H4、C4H6 | D. | C2H4、CH4、C3H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 250mL | B. | 200 mL | C. | 100 mL | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将混有HCl的Cl2通入盛有饱和NaHCO3溶液的洗气瓶除去 | |
| B. | 实验室制取Cl2,浓盐酸起到酸性和还原剂的作用 | |
| C. | 用惰性电极电解饱和食盐水的离子方程式为2Cl-+2H+$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑ | |
| D. | 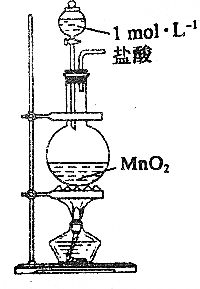 实验室可用图所示装置于制取少量Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上用电解熔融氧化物的方法制备C单质 | |
| B. | 离子半径:C>D | |
| C. | 熔融它们的单质,所克服的微粒间作用力都相同 | |
| D. | 含D的盐溶液都显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
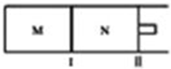 如图所示,隔板I固定不动,活塞II可自由移动,M、N两个容器中均发生反应:A(g)+2B(g)?xC(g),向M、N中通入1mol和2molB的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )
如图所示,隔板I固定不动,活塞II可自由移动,M、N两个容器中均发生反应:A(g)+2B(g)?xC(g),向M、N中通入1mol和2molB的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )| A. | 若x=3,达到平衡后A的体积分数关系为:φ(M)>φ(N) | |
| B. | 若x<3,C的平衡浓度关系为:c(M)<c(N) | |
| C. | 若x>3,达到平衡后B的转化率关系为:α(M)>α(N) | |
| D. | x不论为何值,平衡时M、N中的平均相对分子质量都相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl的电子式: | |
| B. | HClO的结构式为:H-Cl-O | |
| C. | 氯化镁的电子式: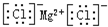 | |
| D. | 用电子式表示氯化氢分子的形成过程: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与浓硝酸、浓硫酸水浴加热并保持55~60℃反应生成硝基苯 | |
| B. | 乙醇在浓硫酸作催化剂和脱水剂且加热至170℃时发生消去反应生成乙烯 | |
| C. | 溴乙烷在氢氧化钠醇溶液中加热发生消去反应生成乙烯 | |
| D. | 甲苯与氯气在光照下反应主要生成2,4二氯甲苯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com