
���� ��1����NaHCO3��Һ�м���NaHSO4��Һ��Ӧ���������ƺ�ˮ��������̼��
��2����FeCl3��Һ�м��백ˮ���߷�Ӧ�����Ȼ�狀�����������
��3��д����ϡ������ϴ���⣨Fe2O3������Ӧ������������ˮ��
��4��Cu2++2OH-=Cu��OH��2�� ���Ա�ʾ�Ȼ�ͭ���������Ʒ�Ӧ��
��� �⣺��1����NaHCO3��Һ�м���NaHSO4��Һ��Ӧ���������ƺ�ˮ��������̼�����ӷ���ʽ��HCO3-+H+=H2O+CO2����
�ʴ�Ϊ��HCO3-+H+=H2O+CO2����
��2����FeCl3��Һ�м��백ˮ���߷�Ӧ�����Ȼ�狀��������������ӷ���ʽ��Fe3++3NH3��H2O�TFe��OH��3��+3NH4+��
�ʴ�Ϊ��Fe3++3NH3��H2O�TFe��OH��3��+3NH4+��
��3��д����ϡ������ϴ���⣨Fe2O3������Ӧ������������ˮ�����ӷ���ʽ��Fe2O3+6H+=3H2O+2Fe3+��
�ʴ�Ϊ��Fe2O3+6H+=3H2O+2Fe3+��
��4��Cu2++2OH-=Cu��OH��2�� ���Ա�ʾ�Ȼ�ͭ���������Ʒ�Ӧ����ѧ����ʽ��CuCl2+2NaOH=Cu��OH��2��+2NaCl��
�ʴ�Ϊ��CuCl2+2NaOH=Cu��OH��2��+2NaCl��
���� ���⿼�������ӷ���ʽ����д����ȷ��Ӧʵ�ʣ���Ϥ���ӷ���ʽ��д�����ǽ���ؼ���ע�⻯ѧʽ��֣�ע�����ӷ�Ӧ��ѭ����ʵ����Ŀ�ѶȲ���


 Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д� �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
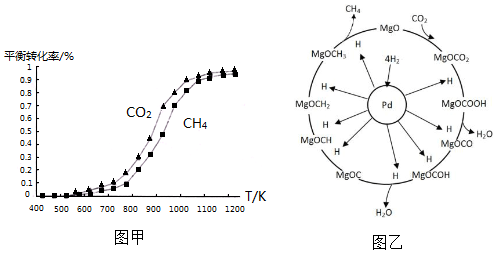 ��ͬ�¶���CO2��ƽ��ת���ʴ��ڣ�����ڡ���С�ڡ���CH4��ƽ��ת���ʣ���ԭ����CO2��������������Ӧ��
��ͬ�¶���CO2��ƽ��ת���ʴ��ڣ�����ڡ���С�ڡ���CH4��ƽ��ת���ʣ���ԭ����CO2��������������Ӧ�� CH4+2H2O��
CH4+2H2O��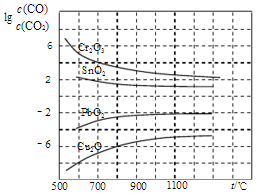
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȩ���Ľṹ��ʽ-COH | B�� | �۱�ϩ�Ľṹ��ʽ 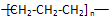 | ||
| C�� | ���Ȼ�̼���ӵĵ���ʽ 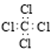 | D�� | ������ӵ����ģ�� 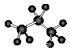 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
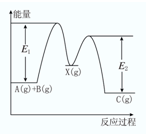 ��ӦA��g��+B��g����C��g����H�����������У���A��g��+B��g����X��g����H1����X��g����C��g����H2����Ӧ�����������仯��ͼ��ʾ��E1��ʾA��g��+B��g����X��g���Ļ�ܣ�����˵����ȷ���ǣ�������
��ӦA��g��+B��g����C��g����H�����������У���A��g��+B��g����X��g����H1����X��g����C��g����H2����Ӧ�����������仯��ͼ��ʾ��E1��ʾA��g��+B��g����X��g���Ļ�ܣ�����˵����ȷ���ǣ�������| A�� | ��H=E1-E2 | B�� | E1�Ƿ�Ӧ�ٵĻ�� | ||
| C�� | X�Ƿ�ӦA��g��+B��g����C��g���Ĵ��� | D�� | ��H2��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | �ߢ�� | C�� | �ۢߢ� | D�� | �ߢ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 50mL 1 mol•L-1 NaCl��Һ | B�� | 100mL2 mol•L-1 AlCl3��Һ | ||
| C�� | 100mL1 mol•L-1 NH4Cl��Һ | D�� | 150mL2 mol•L-1 KCl��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������������Һ��Ӧ������������� | |
| B�� | ���������߲�Ҫ�����ʱά����C����ʧС | |
| C�� | ��֬��������ø�Ĵ�������ˮ��Ϊ������ | |
| D�� | ������ʳ�ؽ��������ӣ�Ӧ�����ȴ���ţ�������ⶾ�ԣ��Լ������嵰�����ж��ij̶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
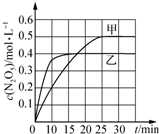 �������������������������������ӦΪ��2NO2��g��+O3��g��?N2O5��g��ʮO2��g����H����ͬ�¶��£������������з���������Ӧ�������Ϣ�����ͼ��ʾ��
�������������������������������ӦΪ��2NO2��g��+O3��g��?N2O5��g��ʮO2��g����H����ͬ�¶��£������������з���������Ӧ�������Ϣ�����ͼ��ʾ��| ���� | �� | �� | �� |
| �ݻ�/L | 1 | 1 | 2 |
| ��Ӧ�� | |||
| ��ʼ�� | 2mol NO2 | ||
| 1mol O3 | 2mol NO2 | ||
| 1mol O3 | 2mol N2O5 | ||
| 1mol O2 | |||
| �¶�/K | T1 | T2 | T2 |
| A�� | 0��10 min�ڼ������з�Ӧ��ƽ�����ʣ�v��NO2��=0.02 mol•L-1•min-1 | |
| B�� | T1��T2����H��0 | |
| C�� | ƽ��ʱN2O5Ũ�ȣ�c����N2O5����c����N2O5�� | |
| D�� | T1Kʱ������ʼʱ���������г���2 mol NO2��1 mol O3��2 mol N2O5��2 mol O2����������Ӧ�ﵽƽ��ǰ��v��������v���棩 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com