
| A. | 1.2mL,NO | B. | 2.4mL,O2 | C. | 3.5mL O2 | D. | 4mL,NO |
分析 NO2和O2的混合气体和水反应方程式有4NO2+O2+2H2O=4HNO3、3NO2+H2O=2HNO3+NO,最后剩余气体可能是NO也可能是O2,根据方程式进行计算.
解答 解:NO2和O2的混合气体和水反应方程式有4NO2+O2+2H2O=4HNO3、3NO2+H2O=2HNO3+NO,最后剩余气体可能是NO也可能是O2,
假设剩余气体是氧气,则只发生反应4NO2+O2+2H2O=4HNO3,根据方程式知,二氧化氮和氧气按体积比为4:1反应,则参加反应的氧气体积=$\frac{(12-2)mL}{5}×1$=2mL,原来氧气体积=(2+2)mL=4mL;
如果剩余是NO,发生的反应为4NO2+O2+2H2O=4HNO3、3NO2+H2O=2HNO3+NO,根据3NO2+H2O=2HNO3+NO得二氧化氮和水反应消耗二氧化氮体积=$\frac{2mL}{1}×3$=6mL,剩余6mL气体中二氧化氮和氧气恰好反应,发生的反应为4NO2+O2+2H2O=4HNO3,则氧气体积=$\frac{6mL}{5}×1$=1.2mL,
故选A.
点评 本题考查混合物的有关计算,明确物质发生的反应是解本题关键,采用差量法进行分析解答,注意利用剩余气体成分进行讨论分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | KOH、Ba(NO3)2、K2CO3、HNO3 | B. | Ba(NO3)2、K2CO3、HNO3、KOH | ||
| C. | KOH、K2CO3、Ba(NO3)2、HNO3 | D. | K2CO3、KOH、Ba(NO3)2、HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钙的化学式是Ca2O2 | |
| B. | 1mol过氧化钠和过氧化钙的混合物中,阴影离子数个数比为1:2 | |
| C. | 过氧化钙与足量水反应生成0.5mol氧气时,转移的电子数为2NA | |
| D. | 过氧化钠和过氧化钙都可作漂白剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
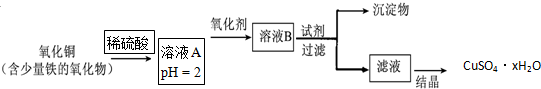

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验目的 | 操作 | 实验现象 | 结论 |
| 1检验Cl- | 取少许滤液于试管中,加入硝酸酸化的硝酸银溶液 | 有白色沉淀产生 | 含有Cl- |
| 2检验NH4+ | 取少许滤液于试管中,加入浓氢氧化钠溶液并加热,将润湿的红色石蕊试纸置于试管口附近 | 石蕊试纸变蓝色 | 含有NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com