
【题目】某课外小组分别用图中所示装置对原电池和电解原理进行实验探究。
请回答:
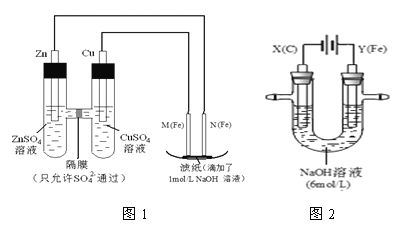
Ⅰ.用甲图装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是________(填序号)。
A.铝 B.石墨 C.银 D.铂
(2)N极为_______(填 “正” “负” “阴” “阳”)电极,发生反应的电极反应式为__________。
(3)实验过程中,SO42-________(填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有_____。
Ⅱ.用乙图装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料得知,高铁酸根离子(FeO![]() )在溶液中呈紫红色,且需碱性环境才可产生。
)在溶液中呈紫红色,且需碱性环境才可产生。
(4)电解过程中,X极区溶液的pH________(填“增大”“减小”或“不变”)。
(5)电解过程中,Y极发生的电极反应为_______________和____________________。
(6)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少________g。
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn===Fe2O3+ZnO+2K2ZnO2。该电池正极发生的反应的电极反应式为__________________________________。
【答案】 A 阴 2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-) 从右向左 滤纸上有红褐色斑点产生(答出“红褐色斑点”或“红褐色沉淀”即可) 增大 Fe-6e-+8OH-=FeO42-+4H2O 4OH--4e-=2H2O+O2↑ 0.28 2FeO42-+6e-+5H2O=Fe2O3+10OH-
【解析】(1)在保证电极反应不变的情况下,仍然是锌作负极,则正极材料必须是不如锌活泼的金属或导电的非金属,铝是比锌活泼的金属,所以不能代替铜,故选A;
(2)N电极连接原电池负极,所以是电解池阴极,阴极上氢离子得电子发生还原反应,电极反应式为:2H++2e-═H2↑(或2H2O+2e-═H2↑+2OH-),故答案为:2H++2e-═H2↑(或2H2O+2e-═H2↑+2OH-);
(3)原电池放电时,阴离子向负极移动,所以硫酸根从右向左移动,电解池中,阴极上氢离子得电子生成氢气,阳极上铁失电子生成亚铁离子,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁被氧气氧化生成氢氧化铁,所以滤纸上有红褐色斑点产生,故答案为:从右向左,滤纸上有红褐色斑点产生;
(4)电解过程中,阴极上氢离子放电生成氢气,则阴极附近氢氧根离子浓度大于氢离子溶液,溶液呈碱性,溶液的pH增大,故答案为:增大;
(5)铁是活泼金属,电解池工作时,阳极上铁失电子发生氧化反应,氢氧根离子失电子发生氧化反应,所以发生的电极反应式为:Fe-6e-+8OH-═FeO42-+4H2O和4OH--4e-═2H2O+O2↑,故答案为:Fe-6e-+8OH-═FeO42-+4H2O;4OH--4e-═2H2O+O2↑;
(6)X电极上析出的是氢气,Y电极上析出的是氧气,且Y电极失电子进入溶液,设铁质量减少为xg,根据转移电子数相等有: ![]() ×2=
×2=![]() ×4+
×4+![]() ×6,x=0.28,故答案为:0.28g;
×6,x=0.28,故答案为:0.28g;
(7)正极上高铁酸根离子得电子发生还原反应,反应方程式为2FeO42-+6e-+5H2O═Fe2O3+10OH-,故答案为:2FeO42-+6e-+5H2O═Fe2O3+10OH-。


科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:

采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2=Na2S2O5。
(1)加试剂前要进行的操作是_______________。
(2)浓硫酸_______ (填“能”或“不能”)用稀硫酸代替,原因是______________。
(3)从装置Ⅱ中分离出产品可采取的分离方法是_____。
(4)为了完整实验装置,在下列装置中选择一个最合理的装置放在装置Ⅲ处,可选用的装置(夹持仪器已略去)为___________(填序号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表。下列判断不正确的是( )

A. a=6.00
B. 同时改变反应温度和蔗糖的浓度,v可能不变
C. b<318.2
D. 不同温度时,蔗糖浓度减少一半所需的时间相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.标准状况下有①6.72L CH4;②3.011023个HCl分子;③7.2gH2O,下列对这三种物质的关系从小到大的排列顺序是:(填写序号)
(1)物质的量______; (2)体积______;
(3)质量______; (4)氢原子数______。
Ⅱ.按要求写出相应的式子:
(1)过氧化钠与水反应的化学方程式:____________________________________;
(2)实验室制取氯气的离子方程式:______________________________________;
(3)铜与稀硝酸反应的离子方程式:______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是离子反应,又是氧化还原反应的是( )
A.Zn 粒与稀硫酸反应制取氢气
B.二氧化碳与氢氧化钠溶液反应生成碳酸钠
C.氧化铁在高温下与一氧化碳反应
D.碳酸钠溶液与石灰乳混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于某些离子的检验及结论一定正确的是
A. 加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32—
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
C. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
D. 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某混合物含有A单质与化合物B,在一定条件下可按图所示发生转化。
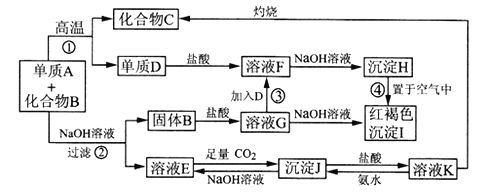
(1)沉淀H变沉淀I的化学方程式_____________________________。
(2)反应②的化学方程式_____________________________。
(3)溶液E中通入过量二氧化碳的离子方程式_______________________________。
(4)用化学反应方程式和简洁的语言解释图中溶液K制取化合物C的过程: __________。
(5)若要保存F溶液,应向溶液中加入两种物质为:_________、________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com