
阿司匹林(乙酰水杨酸)已应用百年,成为医药史上三大经典药物之一,至今它仍是世界上应用最广泛的解热、镇痛和抗炎药,也是作为比较和评价其他药物的标准制剂。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成该物质,设计的合成路线为:
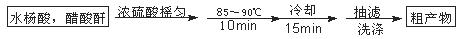
一、制备
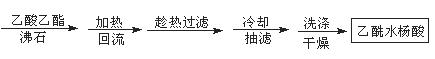
二、提纯
方案1

方案2
主要试剂和产品的物理常数
| 名 称 | 相对分子质量 | 熔点或沸点(0C) | 水 | 醇 | 醚 |
| 水杨酸 | 138 | 158(熔点) | 微溶 | 易溶 | 易溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 反应 | 可溶 | 易溶 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 | 可溶 | 微溶 |
请根据以上信息回答下列问题:
 (1)①合成阿斯匹林时,还会生成一些副产品,其中有一种是高分子,为了分离此物质,方案1中加入A物质为 溶液。
(1)①合成阿斯匹林时,还会生成一些副产品,其中有一种是高分子,为了分离此物质,方案1中加入A物质为 溶液。
②本方案抽滤 后进行洗涤,其具体操作是 。
后进行洗涤,其具体操作是 。
(2)方案2为改进的提纯方法,称为重结晶提纯法。
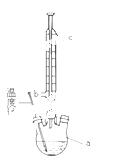
①步骤2回流的装置如图所示,写出仪器a的名称 ,使用温度计的目的是 ,冷凝水的流向为 。
②方案2所得产品的有机杂质要比方案1少的原因是 。
(3)该学习小组在实验中原料用量:2.0g水杨酸、5.0ml醋酸酐(ρ=1.08g·cm-3),最终称量产品m=2.2g ,则乙酰水杨酸的产率为 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
普罗加比对瘫痫、痉挛和运动失调均有良好的治
疗效果,其结构如下图所示,有关普罗加比的说法正确的是
A.该分子在1H核磁共振谱中有12个峰
B.久置在空气中的普罗加比会因氧化而变质
C.1 mol普罗加比最多可与3 mol NaOH反应
D.一定条件下,1mol普罗加比最多能与2mol H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氨基酸可发生如下反应: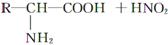
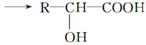
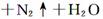 且已知:D、E的相对分子质量分别为162和144,可发生如下物质转化关系,如下图所示:
且已知:D、E的相对分子质量分别为162和144,可发生如下物质转化关系,如下图所示:
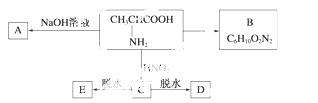
(1)写出B、D的结构简式:B____________,D___________________________。
(2)写出C→E的化学方程式:__________________________________________。
(3)写出C→D的化学方程式:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某物质的结构为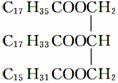 ,关于该物质的叙述正确的是 ( )
,关于该物质的叙述正确的是 ( )
A.一定条件下与氢气反应可以生成硬脂酸甘油酯
B.一定条件下与氢气反应可以生成软脂酸甘油酯
C.与氢氧化钠溶液混合加热能得到肥皂的主要成分
D.与其互为同分异构体且完全水解后产物相同的油脂有三种
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式C4H8O2的有机物与稀硫酸溶液共热可得有机物A和B。将A氧化最终可得C,且C和B为同系
物, 若C可发生银镜反应,则原有机物的结构简式为( )
A.HCOOCH2CH2CH3 B.CH3COOCH2CH3
C.CH3CH2COOCH3 D.HCOOCH(CH3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。
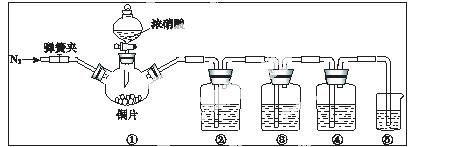
可选药品:稀硝酸、浓硝酸、浓硫酸、NaOH 溶液、蒸馏水
溶液、蒸馏水
查阅资料:
A.浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。
B.氢氧化钠溶液不与NO反应,能与NO2反应2NO2 + 2NaOH = NaNO3 + NaNO2 +H2O
| 实验过程 | 实验现象 |
| I.检验装置的气密性 | |
| II.…… | |
| III.打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞。 | ①中产生大量的红棕色气体,红棕色气体在②中变为无色,气体通过③后依然为无 |
(1)①中发生反应的离 子方程式是 。
子方程式是 。
(2)②中发生反应的化学方程式是 。
(3)装置②~⑤中盛放的药品分别是②  、③ 、④ 、⑤
、③ 、④ 、⑤  。
。
(4)II的操作是 ,目的是 。
(5)该同学得出结论 所依据的实验现象是 。
所依据的实验现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
pH相同的氨水、NaOH和Ba(OH)2溶液,分别用蒸馏水稀释到原来的X、Y、Z倍,稀释后三种溶液的pH仍然相同,则X、Y、Z的关系是( )
A.X=Y=Z B.X>Y=Z
C.X<Y=Z D.X=Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备BaCl2的工艺流程图如下:
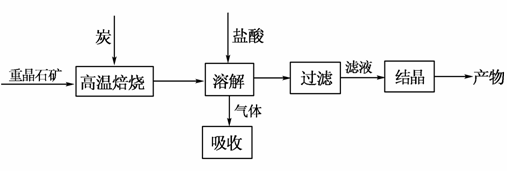
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaSO4(s)+4C(s)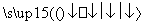 4CO(g)+BaS(s)
4CO(g)+BaS(s)
ΔH1=+571.2 kJ·mol-1 ①
BaSO4(s)+2C(s)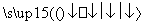 2CO2(g)+BaS(s)
2CO2(g)+BaS(s)
ΔH2=+226.2 kJ·mol-1 ②
(1)气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为________________________________________________。
(2)反应C(s)+CO2(g)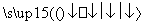 2CO(g)的ΔH=________kJ·mol-1。
2CO(g)的ΔH=________kJ·mol-1。
(3)实际生产中必须加入过量的炭,同时还要通入空气,其目的是______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,将A2和B2气体通入1 L密闭容器中,反应按下式进行:mA2+nB22C,2 s内反应速率如下:v(A2)=0.5 mol·L-1·s-1,v(B2)=1.5 mol·L-1·s-1,v(C)=1 mol·L-1·s-1,则m和n的值分别为( )
A.2、3 B.3、2
C.3、1 D.1、3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com