
| A. | 1项 | B. | 2项 | C. | 3项 | D. | 4项 |
分析 ①依据n=$\frac{m}{M}$计算碳酸钠的物质的量,1mol碳酸钠含有2mol钠离子,据此解答;
②碳酸氢根离子为弱酸的酸式根离子,水溶液中部分水解;
③胶粒是一定数目粒子的集合体;
④氮气与氢气反应为可逆反应,不能进行到底.
解答 解:①106g碳酸钠晶体物质的量为$\frac{106g}{106g/mol}$=1mol,含有2mol钠离子和1mol碳酸给离子,共含有离子总数为3NA,故正确;
②100mL 1mol/LNaHCO3溶液,碳酸根离子部分水解,所以含有小于0.1NA个HCO3-,故错误;
③胶粒是一定数目粒子的集合体,将2 mL 0.5 mol/L硅酸钠溶液滴入盐酸中制得硅酸胶体,所含胶粒数目小于0.001NA,故错误;
④氮气与氢气反应为可逆反应,不能进行到底,所以0.1mol氮气和0.1mol氢气,一定条件下充分反应后转移的电子数小于0.6NA,故错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的判断及计算,熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等之间的转化关系是解题关键,注意盐类水解规律,胶体的性质,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 配位体是Cl-和H2O,配位数是9 | |
| B. | 中心离子是Ti3+,形成配位键时提供电子对 | |
| C. | 配离子是[TiCl(H2O)5]2+,内界和外界中的Cl-的数目比是1:2 | |
| D. | 向含1 mol该配合物的水溶液中加入足量AgNO3溶液,生成AgCl沉淀3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | NaOH的物质的量浓度:c(NaOH)=0.1mol•L-1 | |
| B. | a和b曲线上的任何一点都有:c(Na+)+c(H+)=c(Cl-)+c(OH-) | |
| C. | P点溶液中:c(Na+)=c(Cl-)>c(H+)=c(OH-) | |
| D. | 曲线b是氢氧化钠溶液中逐滴加入盐酸的pH值变化曲线 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
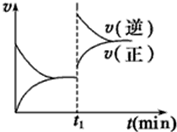 如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强,速率的变化都符合的示意图的反应是( )
如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强,速率的变化都符合的示意图的反应是( )| A. | 2SO2(g)+O2(g)?2SO3(g);△H<0 | B. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g);△H<0 | ||
| C. | H2(g)+I2(g)?2HI(g);△H>0 | D. | N2(g)+3H2(g)?2 NH3(g)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
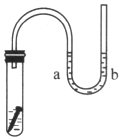 如图所示,试管中放一枚铁钉,并盛放一定量的NaCl溶液,导管中有少量蒸馏水.
如图所示,试管中放一枚铁钉,并盛放一定量的NaCl溶液,导管中有少量蒸馏水.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiCl4晶体是分子晶体 | |
| B. | 常温常压下SiCl4是气体 | |
| C. | SiCl4的分子 是由极性键形成的非极性分子 | |
| D. | SiCl4的熔点高于CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL2mol•L-1的KCl溶液 | B. | 75mL4mol•L-1的NH4Cl溶液 | ||
| C. | 75mL1.5mol•L-1MgCl2溶液 | D. | 150mL1mol•L-1的NaCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com