
| A. | SO2、SiO2、CO、P2O5都是非金属元素形成的氧化物,均为酸性氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有氧化性,都是氧化性酸 | |
| C. | BaCl2、Ca(OH)2、HNO3、HT 均为化合物 | |
| D. | HF、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
分析 A、只能和碱反应生成盐和水的氧化物为酸性氧化物;
B、氧化性体现在中心元素上的、氧化性非常强的酸为氧化性酸;
C、由两种或以上元素构成的纯净物为化合物;
D、在水溶液中或熔融状态下能导电的化合物为电解质.
解答 解:A、只能和碱反应生成盐和水的氧化物为酸性氧化物,而CO不能和碱反应生成盐和水,故不是酸性氧化物,故A错误;
B、氧化性体现在中心元素上的、氧化性非常强的酸为氧化性酸,HClO、H2SO4(浓)、HNO3都是氧化性酸,故B正确;
C、由两种或以上元素构成的纯净物为化合物,而HT是只由一种元素形成的纯净物,故为单质,不是化合物,故C错误;
D、在水溶液中或熔融状态下能导电的化合物为电解质,常见的电解质包括酸、碱、盐、金属氧化物和水等,而乙醇为非电解质,故D错误.
故选B.
点评 本题考查了酸性氧化物、氧化性酸、化合物和电解质的辨别,难度不大,掌握概念的要点是解题关键,同时应注意酸均有氧化性,但不一定是氧化性酸.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:实验题
 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
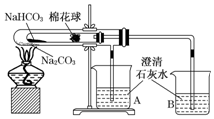 “套管实验”是将一个较小的玻璃仪器装入另外一个玻璃仪器中,经组装来完成原来需要两只或更多普通玻璃仪器进行的实验.因其具有许多优点,近年被广泛开发并应用于化学实验中.下述实验为“套管实验”,请观察如图所示实验装置,分析实验原理,回答下列问题:
“套管实验”是将一个较小的玻璃仪器装入另外一个玻璃仪器中,经组装来完成原来需要两只或更多普通玻璃仪器进行的实验.因其具有许多优点,近年被广泛开发并应用于化学实验中.下述实验为“套管实验”,请观察如图所示实验装置,分析实验原理,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | IBr只作氧化剂 | B. | IBr只作还原剂 | ||
| C. | IBr既不是氧化剂,又不是还原剂 | D. | IBr既是氧化剂,又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原剂与氧化剂的物质的量之比为3:1 | |
| B. | H2O既不作氧化剂又不作还原剂 | |
| C. | 每生成1 mol SO2转移4 mol电子 | |
| D. | S2Cl2只作氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量SO2通入足量NaOH溶液中:SO2+2OH-═SO32-+H2O | |
| B. | 将氨通入稀硫酸中:NH3+H+═NH4+ | |
| C. | 在NaOH溶液中滴入NH4Cl溶液并加热:NH4+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O | |
| D. | 向Ba(OH)2溶液中加入稀H2SO4恰好完全反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com