
【题目】下列图示与对应的叙述相符的是

A.图1表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线II为盐酸,且a点溶液的导电性比b点弱
B.图2表示常温时用0.1000mol·L-1NaOH溶液滴定20.00mL 0.1000mol·L-1CH3COOH溶液所得到的滴定曲线
C.图3表示压强对反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
D.据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO,调节PH在4左右
【答案】D
【解析】
A.醋酸是弱电解质,在水溶液里存在电离平衡,加水稀释促进醋酸电离,溶液的导电性与溶液中离子浓度成正比;
B.醋酸是弱电解质,在水溶液里存在电离平衡,导致溶液中氢离子浓度小于醋酸浓度;
C.该反应是一个反应前后气体体积减小的可逆反应,增大压强平衡向正反应方向移动;
D.根据铁离子的浓度和溶液的pH关系知,当pH=4左右时,铁离子浓度几乎为0,而铜离子还没有开始沉淀。
A.醋酸是弱电解质,在水溶液里存在电离平衡,加水稀释促进醋酸电离,氯化氢是强电解质,完全电离,导致稀释过程中,醋酸中氢离子浓度大于盐酸,所以pH变化小的为醋酸,即II为醋酸,溶液的导电性与溶液中离子浓度成正比,a点导电能力大于b,故A错误;
B.醋酸是弱电解质,在水溶液里存在电离平衡,导致溶液中氢离子浓度小于醋酸浓度,所以未滴定时,0.1000mol·L-1CH3COOH溶液中,醋酸的pH>1,故B错误;
C.该反应是一个反应前后气体体积减小的可逆反应,增大压强平衡向正反应方向移动,则反应物的含量减少,该图中改变条件后,反应物的含量不变,说明平衡不移动,加入的是催化剂,故C错误;
D.加入CuO使溶液中的c(H+)减小,c(OH-)浓度增大,使溶液中c(Fe3+)×c3(OH-)>KSP(Fe(OH)3,使Fe3+生成沉淀而除去,故D正确;
故答案选D。


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
【题目】一种白色晶体A极易溶于水,将A配成溶液进行如下框图所示的实验,实验现象及转化关系如下列框图所示。A为含硫氮正盐其中硫元素化合价为+4,气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝。试回答下列问题:

(1)写出下列物质化学式:D:__________;F:__________。
(2)写出下列反应的离子方程式:
①A和酸性KMnO4溶液反应__________;
②D和新制氯水:__________。
(3)通过本题的解答,在检验SO42-时,应使用__________。
A.盐酸酸化的BaCl2溶液 B.硝酸酸化的Ba(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下列装置制备并检验Cl2的性质。

下列说法正确的是
A. Ⅰ图中:如果MnO2过量,浓盐酸就可全部被消耗
B. Ⅱ图中:量筒中发生了加成反应
C. Ⅲ图中:生成蓝色的烟
D. Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室从废定影液[含Ag(S2O3)23-和Br-等]中回收Ag和Br2的主要步骤为:向废定影液中加入Na2S溶液沉淀银离子,过滤、洗涤、干燥,灼烧Ag2S制取金属Ag;制取C12并将Cl2通入滤液中氧化Br-,再用苯萃取分液。其中部分实验操作的装置如下图所示:
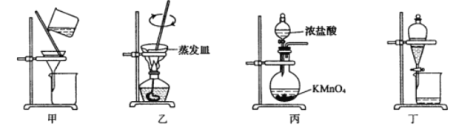
下列叙述正确的是
A. 用装置甲分离Ag2S时,用玻璃棒不断搅拌
B. 用装置乙在通风橱中高温灼烧Ag2S制取Ag
C. 用装置丙制备用于氧化过滤液中Br-的Cl2
D. 用装置丁分液时,先放出水层再换个烧杯继续放出有机层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能。下列有关叙述正确的是
2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能。下列有关叙述正确的是

A.该反应的逆反应为放热反应,升高温度可提高活化分子的百分数
B.该反应中,生成物的总键能大于反应物的总键能
C.该反应的反应热为ΔH= E2- E1使用催化剂改变活化能,但不改变反应热
D.500℃、101kPa下,将1molSO2(g)和0.5molO2(g) 置于密闭容器中充分反应生成SO3(g) 放热xkJ,其热化学方程式为2SO2(g)+O2(g)![]() 2SO3(g)ΔH=-2xkJ·mol-1
2SO3(g)ΔH=-2xkJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯水的叙述,正确的是
A. 新制氯水中只含Cl2和H2O分子
B. 新制氯水可使蓝色石蕊试纸先变红后褪色
C. 光照氯水有气泡逸出,该气体是Cl2
D. 氯水放置数天后酸性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、 Y、Z三种气体的物质的量随时间变化的曲线如图所示:

下列描述正确的是( )
A. 反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)-1
B. 反应开始到l0s,X的物质的量浓度减少了0.79mol/L
C. 反应开始到10s时,Y的转化率为79.0%
D. 反应的化学方程式为:X(g)+Y(g)![]() Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 若反应X + Y = M是放热反应,该反应一定不用加热。
B. 需要加热方能发生的反应一定是吸热反应。
C. 1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热。
D. CO2与CaO化合是放热反应,则CaCO3分解是吸热反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去KCl溶液中少量的MgCl2、MgSO4,可选用Ba(OH)2溶液、盐酸和K2CO3溶液。三种试剂,按下图步骤操作,下列说法错误的是( )
![]()
A.A物质是Ba(OH)2 溶液,为了除尽Mg2+和SO42-
B.B物质是碳酸钠溶液,为了除尽过量的Ba2+
C.C物质是稀盐酸 ,除去过量的CO32-
D.为了除去过量的稀盐酸,加热煮沸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com