
下列反应的离子方程式不正确的是( )
|
| A. | 氯化钡和稀硫酸反应:Ba2++SO42﹣=BaSO4↓ |
|
| B. | 铁与稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
|
| C. | 锌与硫酸铜溶液反应:Zn+Cu2+=Zn2++Cu |
|
| D. | 氢氧化钠和盐酸反应:OH﹣+H+=H2O |
考点:
离子方程式的书写.
分析:
A.硫酸与氯化钡反应生成硫酸钡和氯化氢,硫酸、氯化氢和氯化钡都是强电解质,离子方程式中需要拆开,硫酸钡为难溶物,需要保留化学式;
B.Fe与盐酸反应生成氯化亚铁和氢气,产物错误;
C.锌与硫酸铜发生置换反应,生成硫酸亚铁和Cu;
D.氢氧化钠为可溶性的强碱,盐酸为强酸,二者反应生成可溶性的强电解质氯化钠和弱电解质水.
解答:
解:A.氯化钡和稀硫酸反应生成硫酸钡沉淀和盐酸,反应的化学方程式为H2SO4+BaCl2=BaSO4↓+2HCl,根据离子方程式书写原则,该反应改写成离子方程式为Ba2++SO42﹣=BaSO4↓,故A正确;
B.Fe与盐酸反应生成氯化亚铁和氢气,离子反应为Fe+2H+═H2↑+Fe2+,故B错误;
C.锌和硫酸铜发生置换反应,离子方程式为:Zn+Cu2+=Zn2++Cu,故C正确;
D.稀盐酸与氢氧化钠溶液反应生成氯化钠和水,反应的化学方程式为:HCl+NaOH=NaCl+H2O,氯化氢、氢氧化钠、氯化钠都是易溶物、强电解质,离子方程式中需要拆开,该反应的离子方程式为:OH﹣+H+=H2O,故D正确;
故选B.
点评:
本题考查了离子方程式的正误判别,题目难度不大,试题侧重了基础知识的考查,注意熟练掌握常见反应的化学方程式、离子方程式,明确物质的性质及溶解性、离子方程式的书写规则是解答关键.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:
下列有关实验的叙述,正确的是( )
A. 溴乙烷加氢氧化钠溶液做催化剂加热水解后,再加AgNO3溶液有浅黄色沉淀生成
B. 实验室用分液漏斗分离苯和水的混合物
C. 可以用酸性高锰酸钾溶液除去乙烷中混有的乙烯
D. 除去苯中的少最苯酚,可以先加浓溴水,充分沉淀后过滤即可
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)Z与X形成只含一个中心原子的共价化合物,则它的分子式是 ,其分子的立体结构是 .
(2)Y的最高价氧化物晶体类型是 晶体.X的氧化物与Y的最高氧化物中,分子极性较小的是(填分子式) .
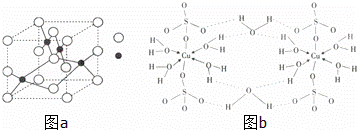
(3)如图a是W的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为 .(图中实心球表示W元素)
(4)铜元素和W元素都位于周期表的ds区,胆矾CuSO4•5H2O可写成[Cu(H2O)4]SO4•H2O,其结构示意图如图b,有关它的说法正确的是 (填字母).
A.该胆矾晶体中存在配位键、共价键和离子键
B.该结构中还存在金属键,极性共价键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(5)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子.已知NF3与NH3的空间构型都是三角锥形,单NF3不易与Cu2+形成配离子,其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列防止金属腐蚀的做法不可行的是( )
|
| A. | 在某些工具的机械转动部位刷油漆 |
|
| B. | 在钢铁中加入铬 |
|
| C. | 在较小钢铁制品的表面包裹塑料 |
|
| D. | 在大型铁壳船的船身上装上一定数量的锌块 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关合金性质的说法正确的是( )
|
| A. | 合金的熔点一般比它的成分金属高 |
|
| B. | 合金的硬度一般比它的成分金属低 |
|
| C. | 组成合金的元素种类相同,合金的性能就一定相同 |
|
| D. | 合金与各成分金属相比,具有许多优良的物理、化学或机械性能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,不说明SO2是酸性氧化物的是( )
|
| A. | 2SO2+O2 | B. | SO2+2NaOH═Na2SO3+H2O |
|
| C. | SO2+H2O⇌H2SO3 | D. | SO2+CaO═CaSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于食品添加剂的叙述中不正确的是( )
|
| A. | 我国应该禁止使用味精 |
|
| B. | 亚硝酸钠可生成致癌物质 |
|
| C. | 醋可同时用作防腐剂和调味剂 |
|
| D. | 苯甲酸钠可用作食品的防腐剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A﹣﹣F六种有机化合物是重要的有机合成原料,结构简式见下表,请根据要求回答下列问题:
| 化合物 | A | B | C |
| 结构简式 |
|
|
|
| 化合物 | D | E | F |
| 结构简式 |
|
|
|
(1)写出符合下列条件的A的同分异构体的结构简式: .
A.核磁共振氢谱有4组峰
B.能发生水解反应
C.在加热条件下能够与新制的氢氧化铜悬浊液生成红色沉淀
(2)化合物B是制取抗心律失常药物﹣﹣氟卡尼的中间体,下列有关描述不正确的是 (填字母).
A.能与氯化铁溶液显色 B.分子中含有羧基、羟基等官能团
C.能与浓溴水反应 D.能与碳酸钠溶液反应产生二氧化碳
(3)化合物B在一定条件下,可以与NaOH溶液发生反应,则1mol化合物B最多需要NaOH的物质的量为 .
(4)化合物C与D在一定条件下发生如下转化得到高分子化合物Z,部分产物已略去.
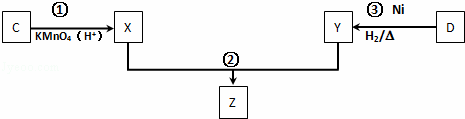
反应③中D与H2按物质的量1:1反应生成Y,则反应②的化学方程式为 .
(5)化合物D与银氨溶液反应的化学方程式(有机物用结构简式表示): .
(6)化合物F是合成克矽平的原料之一,(克矽平是一种治疗矽肺病的药物),其合成路线如下(反应均在一定条件下进行):
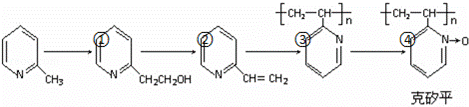
a.反应①是原子利用率100%的反应,则该反应的化学方程式为 ;
b.上述转化关系中没有涉及的反应类型是 (填代号).
①加成反应 ②消去反应 ③还原反应 ④氧化反应 ⑤加聚反应 ⑥取代反应.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com