


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
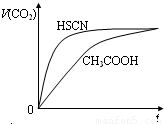
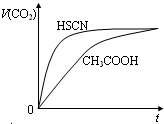 等体积,浓度均为0.1mol/L的三种溶液:①CH3COOH溶液、②HSCN溶液、③NaHCO3溶液,已知将①、②分别与③混合,实验测得产生的CO2气体体积(v)随时间(t)变化的示意图所示,下列说法正确的是( )
等体积,浓度均为0.1mol/L的三种溶液:①CH3COOH溶液、②HSCN溶液、③NaHCO3溶液,已知将①、②分别与③混合,实验测得产生的CO2气体体积(v)随时间(t)变化的示意图所示,下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012年人教版高中化学选修4 3.2水的电离和溶液的酸碱性练习卷(解析版) 题型:选择题
(12分)有甲、乙两份等体积的浓度均为0.1 mol/L的氨水,pH为11.
(1)甲用蒸馏水稀释100倍,则NH3·H2O的电离平衡将向______(选填“促进”或“抑制”)电离的方向移动,溶液的pH将为______(选填序号).
A.9~11之间 B.11
C.12~13之间 D.13
(2)乙用0.1 mol/L的氯化铵溶液稀释100倍,稀释后的乙溶液与稀释后的甲溶液相比较,pH______(选填“甲大”“乙大”或“相等”),其原因是__________________________
________________________________________________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com