
【题目】黄血盐[亚铁氰化钾,K4Fe(CN)6·3H2O]可用作食盐添加剂,一种制备黄血盐的工艺如下所示:

下列说法错误的是
A. HCN溶液有剧毒,含CN-的废水必须处理后才能排放
B. “废水”中含量较多的溶质为CaCl2
C. “试剂 X”可能是K2CO3
D. “系列操作”为蒸发结晶、过滤、洗涤、干燥
科目:高中化学 来源: 题型:
【题目】有关下列四个常用电化学装置的叙述中,正确的是
|
|
|
|
图Ⅰ碱性锌锰电池 | 图Ⅱ铅-硫酸蓄电池 | 图Ⅲ电解精炼铜 | 图Ⅳ银锌纽扣电池 |
A. 图Ⅰ所示电池中,MnO2的作用是催化剂
B. 图Ⅱ所示电池放电过程中,硫酸浓度不断增大
C. 图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学习小组进行如下实验。
【探究反应速率的影响因素】设计了如下的方案并记录实验结果(忽略溶液混合体积变 化)。限选试剂和仪器:0.20mol/LH2C2O4 溶液、0.010mol/L KMnO4 溶液(酸性)、蒸馏水、 试管、量筒、秒表、恒温水浴槽
(1)上述实验①②是探究 对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则 a 为 ;乙是实验需要测量的物理量,则表 格中“乙”应填写 。
【测定 H2C2O4·xH2O 中 x 值】 已知:M(H2C2O4)=90g/mol
称取 1.260 g 纯草酸晶体,将其酸制成 100.00 mL 水溶液为待测液。
②取 25.00 mL 待测液放入锥形瓶中,再加入适的稀 H2SO4
③用浓度为 0.05000 mol·L-1 的 KMnO 标准溶液进行滴定;
(2)请写出与滴定有关反应的离子方程式
(3)某学生的滴定方式(夹持部分略去)如下,最合理的是 (选填 a、b)。
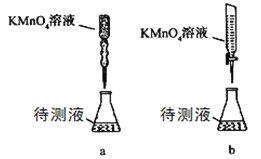
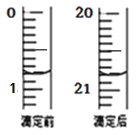
(4)由右图可知消耗 KMnO4 溶液体积为 mL;
(5)滴定过程中眼睛应注视_________________;
(6)通过上述数据,求得 x= 。以标准 KMnO4 溶液滴定样品溶液的浓度,未用 标准 KMnO4 溶液润洗滴定管,引起实验结果 (偏大、偏小或没有影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列说法不正确的是:
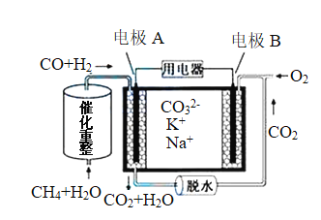
A. 电池工作时,CO32-向电极A移动
B. 电极A上H2参与的电极反应:H2-2e-=2H+
C. 电极B上发生电极反应:O2+2CO2+4e-=2CO32-
D. 反应CH4+H2O=3H2+CO,每消耗22.4 L CH4气体,转移6 mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢卤酸能量关系如图。下列说法不正确的是:
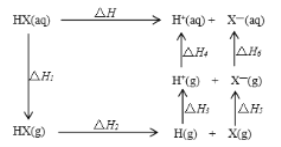
A. 相同条件下,HCl的△H2比HBr的小
B. 已知HF气体溶于水放热,则HF的△H1>0
C. 相同条件下,HCl的△H3+△H4与HI的一样大
D. 一定条件下气态原子生成1 mol H-X键放出a kJ能量,则该条件下△H2=a kJ mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10 mol·L-1的氨水滴定20.00 mL a mol·L-1的盐酸,混合溶液的pH与氨水的体积(V)的关系如图所示。下列说法不正确的是
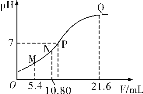
A. 图上四点对应溶液中离子种类相同
B. 若N点溶液中存在c(H+)=c(OH-)+c(NH3·H2O) ,则N点为滴定反应的恰好反应点
C. 图上四点对应的溶液中水的电离程度由大到小排列为N>P>M>Q
D. 若N点为恰好反应点,则M点溶液中存在c(Cl-)=2c(NH3·H2O)+2c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物J是一种常用的抗组胺药物,一种合成路线如下:

已知:①C为最简单的芳香烃,且A、C互为同系物。
②2ROH+NH3![]() HNR2+2H2O(R代表烃基)。
HNR2+2H2O(R代表烃基)。
请回答下列问题:
(1)A的化学名称是______________,H中的官能团名称是________________________。
(2)由D生成E的反应类型是__________,G的结构简式为________________________。
(3)B+C→D的化学方程式为______________。
(4)L是F的同分异构体,含有联苯结构,遇FeCl3溶液显紫色,则L有__________________(不考虑立体异构)种。其中核磁共振氢谱为六组峰,峰面积之比为3∶2∶2∶2∶2∶1的结构简式为______。
(5)写出用氯乙烷和2-氯-1-丙醇为原料制备化合物![]() 的合成路线(其他无机试剂任选) __。
的合成路线(其他无机试剂任选) __。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是一种红褐色液体或黄色气体,其熔点64.5℃,沸点5.5℃,遇水易水解。它是有机合成中的重要试剂,可由NO与Cl2在常温常压下合成。
(1)实验室制备原料气NO和Cl2的装置如下图所示:
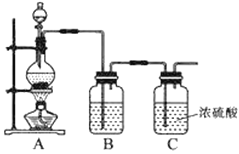
实验室制Cl2时,装置A中烧瓶内发生反应的化学方程式为____。装置B中盛放的试剂为____;
(2)将上述收集到的Cl2充入D的集气瓶中,按图示装置制备亚硝酰氯。
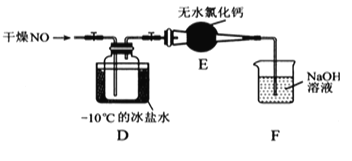
①NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为____。
②装置D中发生的反应方程式为___________________。
③如果不用装置E会引起什么后果_______________
④某同学认为装置F不能有效吸收尾气中的某种气体,该气体为_____,为了充分吸收尾气,可将尾气与____同时通入氢氧化钠溶液中。
(3)工业上可用间接电化学法除去NO,其原理如下图所示,吸收塔中发生的反应为:NO+S2O42+H2O→N2+HSO3
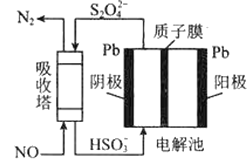
①吸收塔内发生反应的氧化剂与还原剂物质的量之比为_________。
②阴极的电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按如图所示实验装置进行钠跟水反应的实验,据此判断下列说法中正确的是
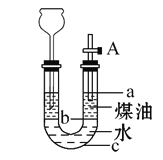
A.打开右端软塞,将一小块金属钠加入煤油中,反应前片刻,钠的位置在a处
B.开始反应后,能观察到的实验现象是钠在b处液面以下的水中反应
C.反应一段时间后,左端液面上升进入长颈漏斗,b处有无色气体产生
D.若用苯或酒精来代替煤油,可观察到相同的实验现象
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com