
| A. | 高价铁盐可用于硬水的软化 | |
| B. | 钾、钠、镁等活泼金属着火时.不能用泡沫灭火器灭火 | |
| C. | 生产水泥和玻璃均可用到碳酸钙 | |
| D. | 石英砂可用干生产粗硅 |
分析 A.硬水软化是指降低水中钙离子、镁离子浓度;
B.过氧化钠、过氧化钾与二氧化碳反应,镁可在二氧化碳中燃烧;
C.根据制取水泥、玻璃的生产中使用的原料来解答;
D.二氧化硅与焦炭反应生成硅与一氧化碳.
解答 解:A.高价铁盐不能降低钙离子、镁离子浓度,所以不能使硬水软化,故A错误;
B.过氧化钠、过氧化钾与二氧化碳反应,镁可在二氧化碳中燃烧,则钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火,一般可用沙子扑灭,故B正确;
C.生产水泥以黏土和石灰石为主要原料,生产玻璃的原料是纯碱、石灰石和石英,均用到碳酸钙,故C正确;
D.二氧化硅与焦炭反应生成硅与一氧化碳,所以石英砂可用于生产单晶硅,故D正确;
故选:A.
点评 本题考查了元素化合物知识,涉及物质的性质及用途,性质决定用途,明确物质的性质是解题关键,注意硬水软化的原理,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5NA | |
| B. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA | |
| C. | 50 mL 18.4 mol•L-1浓硫酸与足量铜加热反应,生成SO2分子的数目为0.46NA | |
| D. | 将含有0.1 mol FeCl3的饱和溶液滴入沸水中,生成的胶体中含胶体粒子的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.4gO2和O3的混合气体,含氧原子数为0.4NA | |
| B. | 分子标准状况下,11.2LCCl4中含分子数为0.5NA | |
| C. | 1mol乙酸(忽视挥发损失)与足量的C2H518OH在浓硫酸作用下加热,充分反应可生成NA个CH3CO18OC2H5 | |
| D. | 常温常压下,7.8gNa2O2含离子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | |||||||
| 三 | ② | ③ | ④ | ⑤ | ⑥ | |||
| 四 | ⑦ | ⑧ |
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
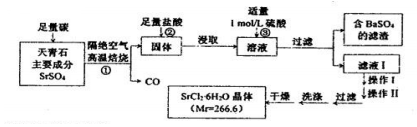
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
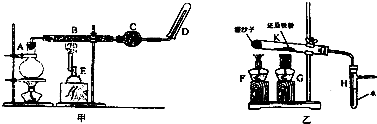
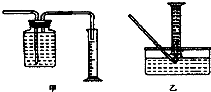
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,2.24 L SO2与O2混合气体中所含氧原子数小于0.2NA | |
| B. | 点解饱和食盐水时,当溶液pH由7变为13,电路中转移的电子数为0.1NA | |
| C. | 常温下,1 L pH=13的Ba(OH)2中含有的OH-数目为0.2NA | |
| D. | 10 mL 98%的H2SO4溶液,加入水中稀释至100 mL,H2SO4的质量分数为9.8% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2 | B. | NO | C. | N2O | D. | N2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于10 s | B. | 等于15 s | C. | 大于15 s | D. | 小于15 s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com