
| A. | 热分解法 | B. | 热还原法 | C. | 电解法 | D. | 置换法 |
分析 在高温条件下利用一氧化碳将铁矿石中的三氧化二铁还原为铁并同时生成了二氧化碳,反应的化学方程式为:3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,依据反应中元素化合价变化解答.
解答 解:在高温条件下利用一氧化碳将铁矿石中的三氧化二铁还原为铁并同时生成了二氧化碳,反应的化学方程式为:3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,在反应中铁元素由+3价降低为0价,发生还原反应,所以此法为:热还原法,
故选:B.
点评 本题考查了金属的冶炼,熟悉金属的活泼性和冶炼方法是解题关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 3.8 g | B. | 4.8 g | C. | 5.4 g | D. | 6.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将40g NaOH溶于1L水中,所得NaOH溶液的浓度为1mol•L-1 | |
| B. | 将2.3g Na投入到97.7g中充分反应,所得溶液中溶质的质量分数为4.0% | |
| C. | 在t℃时,将a g NH3完全溶于水,得到V mL溶液.该溶液的物质的量浓度为$\frac{1000a}{17V}$mol•L-1 | |
| D. | 1mol•L-1的硫酸溶液中c(H+)=1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 草酸能使酸性高锰酸钾溶液褪色 | |
| B. | MnO2、FeCl3和CuSO4都可加快H2O2的分解速率 | |
| C. | 要判断反应进行的方向,必须综合考虑体系的焓变和熵变 | |
| D. | 用稀硫酸和Zn反应制H2时,加少量CuSO4溶液对反应速率无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
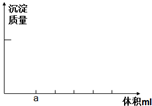 把1.71克硫酸铝配成100ml溶液,为了抑制水解,在配置过程中加入少量硫酸.若在上述溶液中逐滴加入0.5mol/L的氢氧化钠溶液,直至过量.用图象记录滴加过程中产生沉淀的过程.
把1.71克硫酸铝配成100ml溶液,为了抑制水解,在配置过程中加入少量硫酸.若在上述溶液中逐滴加入0.5mol/L的氢氧化钠溶液,直至过量.用图象记录滴加过程中产生沉淀的过程. 
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Fe与足量氧气反应时转移的电子数为2NA | |
| B. | 2L 0.5mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 1mol Na2O2固体中含离子总数为4NA | |
| D. | 丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com