
 在容积相同的不同密闭容器内,分别充入同量的N2和H2,在不同温度,任其发生反应N2+3H2?2NH3,在第7秒时分别测定其中NH3的体积分数φ(NH3),并绘成如图曲线.
在容积相同的不同密闭容器内,分别充入同量的N2和H2,在不同温度,任其发生反应N2+3H2?2NH3,在第7秒时分别测定其中NH3的体积分数φ(NH3),并绘成如图曲线.

 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
| A、pH=6.8的溶液一定显酸性 |
| B、电离平衡常数(K)只与弱电解质本身有关,与其它外部因素无关 |
| C、0.1 mol?L-1的硫化钠溶液中:c(H+)+c(Na+)=c(OH-)+c(HS-)+c(S2-) |
| D、相同物质的量浓度的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,则c(NH4+)由大到小的顺序是:①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | XOH物质的量浓度(mol?L-1) | HCl物质的量浓度(mol?L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH<7 |
| 丁 | 0.1 | 0.1 | pH=5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
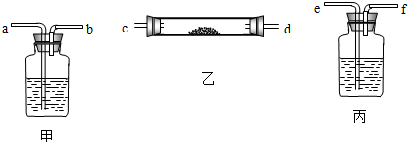
 如图是某学生设计的制取和收集某些气体的实验装置(可加热).
如图是某学生设计的制取和收集某些气体的实验装置(可加热).查看答案和解析>>
科目:高中化学 来源: 题型:
 A:在较高温度下和Br2按物质的量之比1:1发生加成反应的方程式:
A:在较高温度下和Br2按物质的量之比1:1发生加成反应的方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com