
分析 (1)依据氨气密度小于空气密度的物理性质选择排气收集方式;
(2)①根据装置图判断仪器;
②通过蒸馏的方法淡化海水,选择蒸馏装置;
③从食盐溶液中得到食盐晶体,应选择蒸发结晶装置;
④除去食盐水中不溶性的泥沙等杂质,应选择过滤装置.
解答 解:(1)氨气密度小于空气密度,应选择向下排气法收集;
故答案为:下;
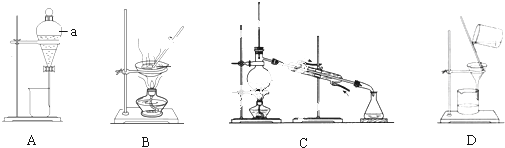
(2)①由图可知,仪器a为分液漏斗,故答案为:分液漏斗;
②通过蒸馏的方法淡化海水,选择蒸馏装置,只有C为蒸馏装置,故答案为:C;
③从食盐溶液中得到食盐晶体,应选择蒸发结晶装置,只有B为蒸发装置,故答案为:B;
④除去食盐水中不溶性的泥沙等杂质,应选择过滤装置,只有装置D符合,故答案为:D.
点评 本题考查了氨气的收集、常见仪器的名称、物质分离提纯方法的选择,熟悉氨气的性质,把握图中装置的作用及混合物分离原理为解答的关键,侧重实验能力及分析能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用焰色反应鉴别NaCl、KCl和Na2SO4 | |
| B. | 用氢氧化钠溶液鉴别MgCl2溶液和AlCl3溶液 | |
| C. | 利用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 | |
| D. | 用加热法鉴别Na2CO3和NaHCO3两种固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
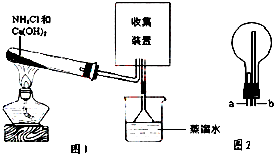 某化学兴趣小组同学用如图所示的实验装置制取氨气并探究氨气的性质,下列有关结论中不正确的是( )
某化学兴趣小组同学用如图所示的实验装置制取氨气并探究氨气的性质,下列有关结论中不正确的是( )| A. | 图1试管中发生反应的化学方程式为:2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O | |
| B. | 向图1烧杯中滴加酚酞溶液,观察到溶液变红,说明氨水呈碱性 | |
| C. | 用图2装置收集氨气时,进气口是a | |
| D. | 图1中的三角漏斗能起到防止氨气倒吸的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠溶液保存在带橡皮塞的玻璃试剂瓶中 | |
| B. | 漂白粉长期放置在烧杯中 | |
| C. | FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| D. | 少量的钠保存在煤油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com