
关于金属物理性质原因的描述不正确的是
| A.金属具有良好的导电性,是因为金属晶体中的“电子气”在电场作用下作定向移动 |
| B.金属具有良好的导热性能,是因为自由电子受热后运动速率增大,与金属离子碰撞频率增大,传递了能量 |
| C.金属晶体具有良好的延展性,是因为金属晶体中的原子层在滑动过程中金属键未破坏 |
| D.金属一般具有银白色光泽,是物理性质,与金属键没有关系 |
科目:高中化学 来源: 题型:单选题
下列化合物,按其晶体的熔点由高到低排列正确的是
| A.SiO2 CaCl2 CBr4CF4 | B.SiO2CsCl CF4CBr4 |
| C.CsCl SiO2 CBr4CF4 | D.CF4CBr4CsCl SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于晶体的叙述中,正确的是
| A.原子晶体中,共价键的键能越大,熔、沸点越高 |
| B.分子晶体中,分子间的作用力越大,该分子越稳定 |
| C.分子晶体中,共价键的键能越大,熔、沸点越高 |
| D.某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某化学式为AB的离子晶体,已知5r(A2+)=4r(B2-)(各类离子晶体与 关系如下图所示),经测定其密度为
关系如下图所示),经测定其密度为 g·cm-3,其摩尔质量为Mg·mol-1,则下列有关该晶体的说法正确的是( )
g·cm-3,其摩尔质量为Mg·mol-1,则下列有关该晶体的说法正确的是( )
| r+/r- | 配位数 | 实例 |
| 0.225~0.414 | 4 | ZnS |
| 0.414~0.732 | 6 | NaCl |
| 0.732~1.0 | 8 | CsCl |
| >1.0 | 12 | CsF |
 cm
cm查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(6)某离子晶体的晶胞结构如图所示。试求: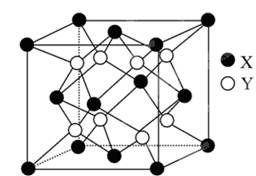
(1)晶体中每一个X同时吸引着________Y,每个Y同时吸引着________个X,该晶体的化学式是________________________。
(2)晶体中在每个X周围与它最接近且距离相等的X共有________个。
(3)晶体中距离最近的2个X与一个Y形成的夹角(∠XYX)为________。
(4)设该晶体的摩尔质量为M g·mol-1,晶体密度为ρ g·cm-3,阿伏加德罗常数为NA,则晶体中两个距离最近的X的核间距离为________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氢气在氯气中燃烧时产生苍白火焰。在反应过程中,破坏1mol氢气中的化学键消耗的能量为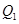 kJ,破坏1mol氯气中的化学键消耗的能量为
kJ,破坏1mol氯气中的化学键消耗的能量为 kJ,形成1mol氯化氢中的化学键释放的能量为
kJ,形成1mol氯化氢中的化学键释放的能量为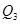 kJ。下列关系式中正确的是( )
kJ。下列关系式中正确的是( )
A.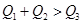 | B.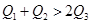 | C. | D.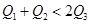 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
干冰晶体是一种面心立方结构,如图所示,即每8个CO2构成立方体,且在6个面的中心各有1个,在每个CO2周围距离为 a(其中a为立方体棱长)的CO2有( )。
a(其中a为立方体棱长)的CO2有( )。
| A.4个 | B.8个 | C.12个 | D.6个 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.7.8克Na2S和Na2O2的固体混合物中含有的阴离子数目为0.1NA |
B.用铜做电极电解CuSO4溶液的反应方程式: 2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
| C.常温时,浓度均为0.01mol/L的 Na2CO3溶液和NaHCO3溶液等体积混合,其溶液中粒子浓度关系为c(CO32-) +c(HCO3-)+c(H2CO3) =0.02mol/L |
| D.在蒸馏水中滴加浓H2SO4,KW不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com