
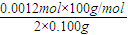 =60%,故答案为:60%;
=60%,故答案为:60%;

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:
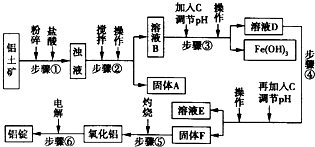
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀pH(离子初始浓度为0.01mol、L) | 4 | 2.3 | 10.4 |
| 完全沉淀pH(离子浓度<10-5mol/L) | 5.2 | 4.1 | 12.4 |
| ||
| 冰晶石 |
| ||
| 冰晶石 |
查看答案和解析>>
科目:高中化学 来源: 题型:
乙醇是我们生活中常接触到的一种有机化合物,根据你学过的乙醇的性质,回答下列有关的问题。
(1)饭店中常使用固体酒精,你判断它应是_______________(纯净物、混合物),质量较差的固体酒精在使用时因燃烧不充分,可能产生有毒气体____________(写分子式)。
(2)在焊接铜漆包线的线头时,常先把线头放在火上烧一下,以除去漆层,并立即在酒精中蘸一下就可得到光亮的铜线头,写出这个过程中发生反应的化学方程式:
________________________________
_________________________________
(3) 用硫酸酸化的CrO3遇酒精后,其颜色会从红色变为蓝绿色,用这个现象可以测得汽车司机是否酒后驾车。反应的化学方程式如下
2CrO3+3C2H5OH+3H2SO4→ Cr2(SO4)3+3CH3CHO+6H2O
该反应中,乙醇发生_________反应(填有机反应类型),
乙醇分子中的__ ____号键断裂(填图中序号),
产物CH3CHO的名称是______________,结构式为____________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山西省山大附中高一5月月考化学试卷(B)(带解析) 题型:填空题
乙醇是我们生活中常接触到的一种有机化合物,根据你学过的乙醇的性质,回答下列有关的问题。
(1)饭店中常使用固体酒精,你判断它应是_______________(纯净物、混合物),质量较差的固体酒精在使用时因燃烧不充分,可能产生有毒气体____________(写分子式)。
(2)在焊接铜漆包线的线头时,常先把线头放在火上烧一下,以除去漆层,并立即在酒精中蘸一下就可得到光亮的铜线头,写出这个过程中发生反应的化学方程式:
________________________________
_________________________________
(3) 用硫酸酸化的CrO3遇酒精后,其颜色会从红色变为蓝绿色,用这个现象可以测得汽车司机是否酒后驾车。反应的化学方程式如下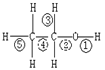
2CrO3+3C2H5OH+3H2SO4→ Cr2(SO4)3+3CH3CHO+6H2O
该反应中,乙醇发生_________反应(填有机反应类型),
乙醇分子中的__ ____号键断裂(填图中序号),
产物CH3CHO的名称是______________,结构式为____________。
查看答案和解析>>
科目:高中化学 来源:2014届山西省高一5月月考化学试卷(B)(解析版) 题型:填空题
乙醇是我们生活中常接触到的一种有机化合物,根据你学过的乙醇的性质,回答下列有关的问题。
(1)饭店中常使用固体酒精,你判断它应是_______________(纯净物、混合物),质量较差的固体酒精在使用时因燃烧不充分,可能产生有毒气体____________(写分子式)。
(2)在焊接铜漆包线的线头时,常先把线头放在火上烧一下,以除去漆层,并立即在酒精中蘸一下就可得到光亮的铜线头,写出这个过程中发生反应的化学方程式:
________________________________
_________________________________
(3) 用硫酸酸化的CrO3遇酒精后,其颜色会从红色变为蓝绿色,用这个现象可以测得汽车司机是否酒后驾车。反应的化学方程式如下

2CrO3+3C2H5OH+3H2SO4 → Cr2(SO4)3+3CH3CHO+6H2O
该反应中,乙醇发生_________反应(填有机反应类型),
乙醇分子中的__ ____号键断裂(填图中序号),
产物CH3CHO的名称是______________,结构式为____________。
查看答案和解析>>
科目:高中化学 来源:期末题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com