
| A. | 向饱和AgCl水溶液中加入盐酸,Ksp(AgC1)变大 | |
| B. | AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-) | |
| C. | 温度一定,当溶液中c(Ag+)c(Cl- )<Ksp(AgCl)时,此溶液中必有AgCl沉淀析出 | |
| D. | 向AgI的悬浊液中加NaCl浓溶液,可能有AgCl生成 |
分析 A.温度不变,难溶物的溶度积不变;
B.当硝酸银和氯化钠的物质的量不相等时,c(Ag+)、c(Cl-)不相等;
C.只有c(Ag+)•c(Cl-)大于Ksp(AgCl)时,才能生成AgCl沉淀;
D.若c(Ag+)•c(Cl-)大于Ksp(AgCl),会生成氯化银沉淀.
解答 解:A.向饱和AgCl水溶液中加入盐酸,由于温度不变,则溶度积Ksp(AgC1)不变,故A错误;
B.AgNO3溶液与NaCl溶液混合后的溶液中,当硝酸银与氯化钠的物质的量相等时一定有c(Ag+)=c(Cl-),若二者的物质的量不相等,则c(Ag+)、c(Cl-)不相等,故B错误;
C.温度一定,当溶液中c(Ag+)•c(Cl-)>Ksp(AgCl)时,此溶液中有AgCl沉淀析出,若c(Ag+)c(Cl-)<Ksp(AgCl),不会析出沉淀,故C错误;
D.向AgI的悬浊液中加NaCl浓溶液,若溶液中c(Ag+)•c(Cl-)>Ksp(AgCl),则会析出AgCl沉淀,故D正确;
故选D.
点评 本题考查了难溶物溶解平衡及其应用,题目难度中等,明确难溶物溶解平衡及其影响因素为解答关键,注意掌握溶度积常数的概念及含义,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①变轻,②变重,③不变 | B. | ①变轻,②不变,③变重 | ||
| C. | ①变轻,②不变,③不变 | D. | ①变重,②不变,③变轻 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol/L H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盛装待测液的锥形瓶用蒸馏水洗过,没用待测液润洗 | |
| B. | 酸式滴定管在使用前未用待测液盐酸润洗 | |
| C. | 滴定前碱式滴定管尖嘴中有气泡,滴定后气泡消失 | |
| D. | 滴定前读数平视,滴定终点读数时俯视碱式滴定管的刻度 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
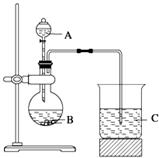
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ②KCl
②KCl (3)H2O2
(3)H2O2 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
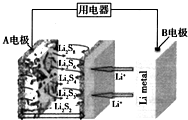
| A. | B电极为正极 | |
| B. | A电极上的电极反应式为:2Li++S8+2e-═Li2S8 | |
| C. | 每生成1molLi2S8转移0.25 mol电子 | |
| D. | 给该电池充电时,A电极连接电源的负极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com