
| A. | 1:1 | B. | 1:2 | C. | 1.87:1 | D. | 3.65:1 |
分析 先利用极值法判断氢氧化钠过量情况,氢氧化钠不足时硫酸氢铵电离出的氢离子优先反应,然后铵根离子与氢氧化钠反应,根据氨气的物质的量可计算出硫酸氢铵的物质的量,然后利用总质量可计算出硫酸铵的质量,最后可计算出混合物中(NH4)2SO4和NH4HSO4的物质的量之比.
解答 解:假设混合物完全为(NH4)2SO4时消耗NaOH的量最小,7.24g(NH4)2SO4的物质的量为:$\frac{7.24g}{132g/mol}$≈0.0548mol,消耗氢氧化钠的物质的量为0.0548mol×2=0.1096mol>0.1mol,说明氢氧化钠的物质的量不足,
(NH4)2SO4和NH4HSO4混合物样品中加入氢氧化钠溶液后,先与反应NH4HSO4,然后与(NH4)2SO4反应生成氨气,标准状况下生成氨气的物质的量为:$\frac{1792×1{0}^{-3}L}{22.4L/mol}$=0.08mol,
则与氢离子反应消耗NaOH的物质的量为:0.1mol-0.08mol=0.02mol,故NH4HSO4的物质的量为0.02mol,
所以(NH4)2SO4的质量为:7.24g-115g/mol×0.02mol=4.94g,其物质的量为:$\frac{4.94g}{132g/mol}$≈0.0374mol,
则(NH4)2SO4和NH4HSO4的物质的量比为:0.0375mol:0.02mol=1.87:1,
故选C.
点评 本题考查了混合物反应的计算,题目难度中等,正确判断氢氧化钠的过量情况及发生反应的先后顺序为解答关键,注意掌握极值法在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| 电离能序号 | I1 | I2 | I3 | I4 |
| 电离能(kJ/mol) | 740 | 1500 | 7700 | 10500 |
| A. | s区 | B. | p区 | C. | d区 | D. | ds区 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
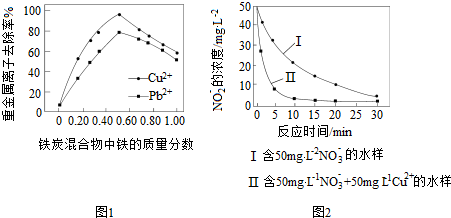
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
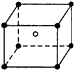
| A. | 1:8 | B. | 1:4 | C. | 1:2 | D. | 1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 和
和 代表不同元素的原子.
代表不同元素的原子.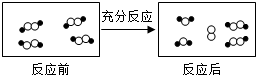
| A. | 一定属于吸热反应 | B. | 一定属于可逆反应 | ||
| C. | 一定属于氧化还原反应 | D. | 一定属于分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
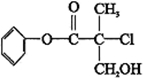
| A. | 有机物A 属于芳香烃 | |
| B. | 有机物A 可以与Br2的CCl4溶液发生加成反应 | |
| C. | 有机物A 与浓硫酸混合加热,可以发生消去反应 | |
| D. | 1 mo1A 与足量的NaOH 溶液反应,最多可以消耗3mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com