
【题目】新型的乙醇电池结构如图所示,它用碘酸类质子溶剂,在200℃左右时供电,其效率比甲醇电池高出32倍,且更安全.已知电池总反应式为C2H5OH+3O2═2CO2+3H2O.下列说法不正确的是( )
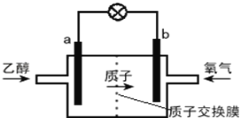
A. a极为电池的负极,该电极发生氧化反应
B. 电池工作时电子由a极流出沿导线经灯泡到b极
C. 电池正极的电极反应式为 O2+2H2O+4e﹣═4OH﹣
D. 电池工作时,1mol乙醇被氧化转移12mol电子
【答案】C
【解析】由质子的定向移动方向可知a为负极,b为正极,负极发生氧化反应,乙醇被氧化生成CO2和H+,电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+,正极氧气得到电子被还原,电极反应式为4H++O2+4e-=2H2O,结合电极反应解答该题.
A、原电池工作时,阳离子向正极移动,则b为正极,a为负极,乙醇在负极失电子发生氧化反应,故A正确;B、原电池中电子从负极流向正极,则电子由a极流出沿导线经灯泡到b极,故B正确;C.酸性条件下,氧气得电子生成水,池工作时,正极的电极反应式为4H++O2+4e-=2H2O,故C错误;D.乙醇被氧化生成CO2和H+,电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+,则1mol乙醇被氧化转移12mol电子,故D正确;故选:C。


科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛。回答下列问题:
(1)生产Na2S2O5,通常是由NaHSO3过饱和溶液经结晶脱水制得。写出该过程的化学方程式__________。
(2)利用烟道气中的SO2生产Na2S2O5的工艺为:

①pH=4.1时,Ⅰ中为__________溶液(写化学式)。
②工艺中加入Na2CO3固体、并再次充入SO2的目的是__________。
(3)制备Na2S2O5也可采用三室膜电解技术,装置如图所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3。阳极的电极反应式为_____________。电解后,__________室的NaHSO3浓度增加。将该室溶液进行结晶脱水,可得到Na2S2O5。

(4)Na2S2O5可用作食品的抗氧化剂。在测定某葡萄酒中Na2S2O5残留量时,取50.00 mL葡萄酒样品,用0.01000 mol·L1的碘标准液滴定至终点,消耗10.00 mL。滴定反应的离子方程式为_____________,该样品中Na2S2O5的残留量为____________g·L1(以SO2计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中,发生可逆反应mA(g)+nB(g)![]() pC(g)+qD(g),当m、n、p、q为任意整数时,不能作为达到平衡标志的是
pC(g)+qD(g),当m、n、p、q为任意整数时,不能作为达到平衡标志的是
A. 体系的压强不再改变B. 体系的温度不再改变
C. 各组分的浓度不再改变D. 各组分的质量分数不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。完成下列各题:
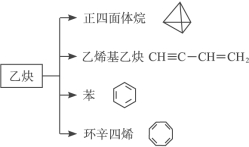
(1)正四面体烷的分子式为____________,其二氯取代产物有____________种。
(2)关于乙烯基乙炔分子的说法错误的是____________。
a.能使KMnO4酸性溶液褪色
b.1 mol乙烯基乙炔能与3 mol Br2发生加成反应
c.乙烯基乙炔分子内含有两种官能团
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:____________。
(4)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例):________________________、______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生配制0.1 mol·L-1氢氧化钠溶液 100 mL,下列操作会造成实际浓度偏高的是( )
A.空盘时天平指针指向左边
B.把烧碱放在滤纸上称量
C.定容时俯视刻度线
D.使用部分变质的烧碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E为原子序数依次增大的5种短周期元素。A是最轻的金属,B的最低负化合价的绝对值比最高正化合价少2,C的简单阴离子C2-与氖原子有相同的电子层结构,D与A同主族,E的M层电子数比L层少2个。
(1)写出元素符号:A______、C______,E在元素周期表中的位置是________________;
(2)C、D、E原子半径由大到小:______(写元素符号,后同),C、D、E简单离子的半径由大到小_____;
(3)A常用作电池的电极材料,含A的电池通常采用非水电解质或固体电解质,原因是______(用化学方程式解释);
(4)B与氢元素可以形成10电子微粒X和18电子微粒Y,Y是一种良好的火箭燃料。X中含有的共价键类型是_______,Y的电子式为_________;
(5)C的两种单质在常温下都是气体,它们互为____________。比较C的氢化物和E的氢化物沸点:C___E(填“>”“<”或“=”),原因是____________
(6)用电子式表示D与E的二元化合物的形成过程:________________,碳原子与E能形成AB2型化合物,请写出该物质的电子式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M是一种香料,可用如下路线合成:

已知:①双键在链端的烯烃发生硼氢化-氧化反应,生成的醇羟基在链端:

②![]()
③A、B发生同一反应类型有机物都只生成C
④核磁共振氢谱显示E分子中有两种氢原子,F为芳香族化合物。
请回答下列问题:
(1)原料C4H10的名称是 _______________(用系统命名法);
(2)写出反应A→C的反应试剂和条件:____________________;
(3)F与新制Cu(OH)2反应的化学方程式 _______________________;
(4)D +G →M反应的化学方程式_________________________;
(5)写出N、M的结构简式 _________________、_________________;
(6)写出与G具有相同官能团的G的所有芳香类同分异构体(不包括G本身)的结构简式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯元素及氯气的叙述中,正确的是( )
A.干燥的氯气可以贮存在钢瓶中
B.氯元素在自然界中既有化合态存在,也有游离态存在
C.氯气难溶于水,可直接用排水法收集氯气
D.氯水、液氯是状态不同的同一种物质,均属于纯净物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com